Автолиз дрожжей
Дрожжевые клетки содержат большой запас ферментов, питательных веществ и множество ароматобразующих веществ, но, прежде чем эти соединения поступят в вино, необходимо, чтобы наступил автолиз дрожжевых клеток.
При автолизе дрожжей нарушается клеточный метаболизм. Под действием Р-1,3-глюконазы и протеолитических ферментов гидролизуются глюкан и маннан, а также протеиды клеточной оболочки, она становится пористой и проницаемой, при этом содержимое клетки диффундирует в окружающую среду.
В результате изменения внутриклеточного pH активность лизирующих ферментов увеличивается. Протеазы вызывают распад белковых ферментов, поэтому они инактивируются. При этом нарушается координационная связь между ферментами и их клеточной регуляцией. Разрушаются субклеточные структуры, распадается также цитоплазматический комплекс белков, липидов и полисахаридов. Следовательно, ферменты также инактивируются, так как они являются протеидами.
В автолизатах, полученных путем нагревания дрожжей, происходит само- переваривание дрожжевых клеток, при этом инактивируются все ферменты. Использование таких автолизатов не столь благоприятно для улучшения качества вина и шампанского, хотя вкус и букет несколько улучшаются за счет ароматобразующих веществ находившихся в самой дрожжевой клетке.
При получении автолизатов с помощью механического разрушения клеток холодом при высоком давлении ферменты дрожжей полностью сохраняются. Полученные таким способом автолизаты усиливают биохимические процессы при созревании вина.
В присутствии ферментов дрожжей в вине усиливаются синтетические процессы, в результате образуются сложные эфиры и внутренние эфиры, так называемые лактоны, а также ароматические спирты. Эстеразы усиливают синтез высокомолекулярных эфиров, линолевой, линоленовой кислот, терпеновых эфиров, линалилацетата, геранилацетата, терпинилацетата, а также энантовых эфиров.
Синтезируются ароматические спирты: β-фенилэтиловый спирт и его ацетатный эфир, тиразол и триптофол. При обработке дрожжей холодом сохраняются терпеноидные соединения, как цис- и транс-фарпезол. Все эти вещества усиливают букет и вкус вина.
Большую роль играет восстановительный фермент глютатион-редуктаза, которая восстанавливает окисленный глютатион и образует окислительно-восстановительную систему окисленный глютатион ↔ восстановленный глютатион. Эта система снижает редокспотенциал вина, при этом происходит восстановление окисленных букетистых веществ, которые улучшают аромат вина.
Неферментативные окислительно-восстановительные процессы и их катализаторы
При отсутствии биологических катализаторов (ферментов) такую роль в окислительно-восстановительных процессах играют тяжелые металлы. Для активирования кислорода воздуха большое значение имеют неорганические катализаторы — железо и медь. При взаимодействии этих катализаторов с перекисью водорода или с другими органическими перекисями выделяется активный кислород, который способен окислить углеводороды, углеводы, аминокислоты и жиры.
Согласно теории Ж. Риберо-Гайона [73], процесс окисления вина представляется следующим образом. Молекулярный кислород не может непосредственно реагировать с компонентами вина. Он реагирует с нестойкими веществами и образует так называемые промежуточные окислители, обладающие большой окислительной способностью. Эти промежуточные окислители, снабженные кислородом, и производят окисление компонентов вина. Ж. Риберо-Гайон считает, что процесс окисления вина протекает в две фазы: первая фаза состоит из присоединения кислорода воздуха к нестойким веществам вина, а во второй фазе нестойкие соединения, нагруженные кислородом, способны окислить трудноокисляемые соединения вина.
Эта теория окисления вина по Ж. Риберо-Гайону аналогична перекисной теории А. Н. Баха. Однако разница заключается в том, что у А. Н. Баха в качестве окислителя служит оксигеназа, а у Ж. Риберо-Гайона — промежуточные окислители.
Согласно современным представлениям, тяжелые металлы также способны активировать молекулярный кислород. Каталитическое действие двухвалентного железа на окисление элементов вина можно представить следующим образом. Инициирование цепных реакций происходит только в присутствии Fe2+ молекулярным кислородом: Fe2+O2↔Fe3++02. При этом образуется супероксид (0*2_ ), который является продуктом одноэлектронного восстановления молекулярного кислорода. Супероксид в кислой среде, какой является вино, присоединяет протон, и переходит в супероксидный радикал НО; участвующий в реакциях гидроксилирования.
При взаимодействии ионов двухвалентного железа с перекисью водорода возникают радикалы НО- и ОН-. Образование свободных радикалов способствует дальнейшему разложению перекиси водорода, при этом возникают длинные цепи реакции
![]()
Эти реакции можно представить в виде последовательного присоединения электронов к кислороду, если в биологической системе присутствуют Fe2+ и О2;
![]()
Радикал НО2 теоретически может образовываться при действии терминальных оксидаз и оксигеназ, поскольку они являются продуктами одноэлектронного восстановления молекулярного кислорода. Образование этих радикалов при окислении-органических соединений молекулярным кислородом катализирует пероксидаза.
Перекисное окисление органических соединений происходит в присутствии ионов двухвалентного железа.
Еще в 1951 г. мы показали, что двухвалентное железо интенсивно окисляет винную кислоту, при этом образуется диоксифумаровая кислота, которая восстанавливает трехвалентное железо в двухвалентное [76]:
![]() >
>
Восстановление двухвалентного железа обусловливает истинный каталитический процесс.
Восстановление трехвалентного железа в двухвалентное происходит также в присутствии аскорбиновой кислоты, восстановленного глютатиона и цистеина. Эти соединения могут непосредственно реагировать со свободными радикалами.
Установлено, что образовавшийся в результате реакции инициирования свободный радикал обладает высокой реакционной способностью. Он активно реагирует с молекулярным кислородом с образованием перекисного радикала (Эмануэль и др., 1965).![]()
Константа скорости (K2) этой реакции очень велика (107—108 моль/с), а энергия активации практически равна нулю, поэтому при концентрации кислорода в системе выше 10-6 MR* превращается в перекисный радикал RO2. Этот радикал в свою очередь взаимодействует с новой молекулой окисляющегося соединения и превращается в гидроперекись (ROOH|), при этом вновь обрадуется радикал R:
![]()
При восстановлении гидроперекиси (ROOH) в присутствии восстановленного глютатиона образуется спирт (ROH).
В дрожжевой клетке этот процесс происходит при участии фермента глютатиопредуктазы. Интересно отметить, что восстановленный глютатион и цистеин оказывают на перекисное окисление комбинированное действие, выступая одновременно как восстановитель трехвалентного железа и гидроперекисей, а также как ингибитор свободных радикалов.
Способностью активировать молекулярный кислород обладают органические оксикислоты с непредельной связью, как, например, диоксифумаровая и аскорбиновая кислоты [120]. Реакция активирования кислорода протекает по следующей схеме: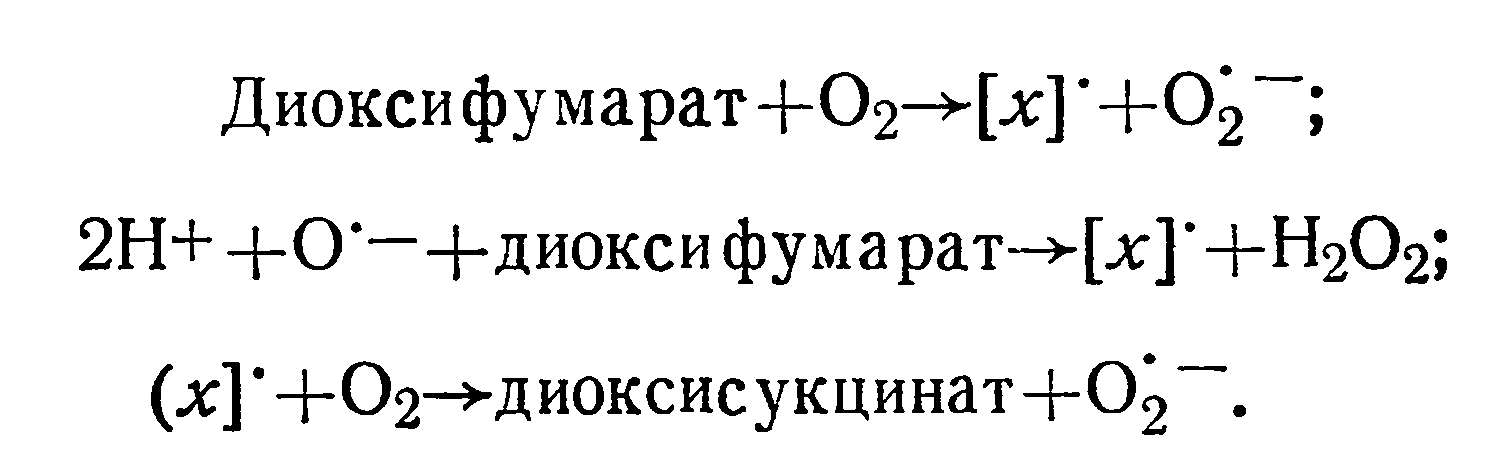
Правильность этих реакций подтверждают следующие наблюдения: если спектр ЭПР [х], возникающий при анаэробных условиях, немедленно исчезает, то в реакцию вступает кислород. Следовательно, диоксифумаровая кислота в
присутствии кислорода активирует его вначале в O2, затем в перекись водорода. [х] — свободный радикал, образованный при потере одного электрона из диоксифумаровой кислоты.
Медь также катализирует окисление диоксифумарата посредством различных механизмов. Однако стимулирование этого процесса происходит посредством Мп2+, так как Мп2+ реагирует с O2, образуя комплекс, обладающий большой каталитической способностью:
![]()
Реакция [O2—+Мn2+] обладает гораздо большей каталитической активностью, чем реакция [диоксифумарат 4- O2→[x] +O-2]. При добавлении пероксидазы скорость окисления диоксифумарата намного увеличивается. Это увеличение зависит главным образом от присутствия супероксида [120].
Супероксиддисмутаза (O2—O-2 оксидоредуктаза) и каталаза (Н2O2 оксидоредуктаза) играют важную роль для защиты от токсических форм кислорода (O2-, ΌΗ·ΟΗ—НO2 и Н2О2Х Действие супероксиддисмутазы на Of превращает его в перекись водорода (O2 +O-2+2Η+→Η2O2+O2). Затем действие каталазы приводит к разложению перекиси водорода до воды и кислорода.
Таким образом, функционирование этих двух ферментов обеспечивает живой клетке достаточно надежную защиту от наиболее токсических форм кислорода.
Для ингибирования протекания окислительных процессов в вине необходимо удалить ионы железа и меди. Это удается осуществить с помощью оклейки вина желтой кровяной солью. Лучшим ингибитором является ЭДТА (этилендиаминтетрауксусная кислота|), которая образует неактивный комплекс с ионами железа.
К неферментативным процессам относятся и процессы меланоидинообразования.
Меланоидины образуются при неэнзиматической реакции путем взаимодействия аминокислот с сахарами, что связано с потемнением вина. В процессе деградации углеводов, а также в результате сахароаминной реакции в кислой среде накапливается большое количество этих веществ. Меланоидины содержат гидроксильные, карбоксильные и карбонильные группировки, а также эфирные связи. Молекулярная масса их колеблется от 2 до 13 тыс.
Многие исследователи изучали реакцию Майяра на различных объектах и выделили производные фурана, пирана, пиррола, пиразина, карбонила и других гетероциклических и ароматических соединений.
Главной реакцией при взаимодействии сахаров с аминокислотами является образование темноокрашенных продуктов — меланоидинов. При этой реакции появляется специфический запах, увеличивается кислотность, выделяется углекислота и повышается восстановительная способность. Появление редуктонов связано с окислением сопряженной диендиоловой структуры, которая способна полимеризироваться с образованием меланоидинов.
Исследования Е. Ходжа (1953) показали, что сахароаминная реакция протекает в три стадии: на первой стадии происходит конденсация аминокислоты с углеводом с образованием N-гликозиламина. При нагревании N-гликозиламин претерпевает внутримолекулярную перегруппировку Амадори и изомеризуется r амин-1-дезокси-2-кетозу.
На втором этапе происходит дегидратация амин-1-дезокси-2-кетона и его распад на более низкомолекулярные соединения: оксиметилфурфурол, фурфурол, диацетил, ацетоин, альдегиды, ацетон, фуран, оксифуран, левулиновую кислоту и другие вещества, участвующие в побурении вина.
По литературным данным, в результате сахароаминной реакции образуется более 50 веществ. На втором этапе сахароаминной реакции происходит распад аминокислот по Штеккеру с образованием альдегидов. Таким образом, один из путей деградации амин-1-дезокси-2-кетоз сопровождается образованием альдегидов, кетонов, спиртов, редуктонов. Альдегиды и редуктоны могут взаимодействовать с аминокислотами, образуя меланоидины с различным химическим строением.
Так, по данным В. Л. Кретовича и Р. Р. Токаревой (1948), при меланоидиновой реакции были выделены с помощью бумажной хроматографии фурфурол, оксиметилфурфурол, альдегиды (уксусный, пропионовый, изомасляный, изовалериановый, коричный, сиреневый, ванилин, параоксибензальдегид, конифериловый).
З. Н. Кишковский [45] среди летучих веществ сахароаминной реакции идентифицировал метанол, этанол, ацетон и альдегиды (уксусный, пропионовый и масляный).
Исследования И. А. Егорова, В. Н. Ломинадзе, А. Ю. Скрипника [35] показали, что в состав вновь образующихся веществ при нагревании до 190°С в течение 2 ч водных растворов сахарозы без добавления аминокислот входят формальдегид, уксусный и масляный альдегиды, ацетон и фурфурол. В присутствии аминокислот эта реакция ускоряется во много раз и количество возникающих продуктов увеличивается. Эти же авторы в другой работе [36] установили, что при нагревании сахарозы с аланином образуются метиловый, этиловый, пропиловый и изобутиловый спирты, а при нагревании сахарозы с фенилаланином, кроме указанных спиртов, возникает еще β-фенилэтиловый.
На конечном этапе меланоидинообразования происходит альдольная конденсация безазотистых соединений с образованием низко- и высокополимерных соединений и альдегидаминная реакция с возникновением гетероциклических соединений. А. Спарк считает, что потемнение различных насыщенных и ненасыщенных альдегидов с аминокислотами приводит к образованию пигментов, не содержащих азота. Монокетозамины являются промежуточными продуктами, включая аминный азот. Они определяют ход реакции при потемнении альдозаминных систем. А. Спарк показал, что наиболее быстро с аминокислотами реагирует ксилоза, затем манноза, галактоза, глюкоза, сорбоза, фруктоза; сахароза и мальтоза почти не реагируют.
Помимо сахаров, в реакции меланоидинообразования принимают участие органические кислоты, альдегиды, кетоны, фенольные соединения и другие вещества. Кроме аминокислот, в этой реакции участвуют амины, пептиды, белки.
Методом гельфильтрации на сефадексе G-75 3. Н. Кишковский, Н. А. Мехузла, Т. А. Сахарова (1966) из конечных продуктов меланоидиновой реакции выделили различные фракции. Было показано, что эти фракции не содержат свободных альдегидов и аминных групп и не реагируют с нингидрином. И. Личев [56] с помощью гельфильтрации на сефадексе разделил продукты меланоидиновой реакции на низкомолекулярные и на полимеры.
А. Спарк приводит схему меланоидинообразования, где показаны пути взаимодействия альдоз и аминокислот, включая образование из дикетозаминов различных дезоксиозонов и карбонильных соединений, которые затем дегидрируются и конденсируются в полимеры.
Более подробную схему образования меланоидинов приводит и Е. Ходжа, которая подробно описана в книге З. Н. Кишковского и И. М. Скурихина [46]. Б. Давидянц [22] предложил гипотетическую схему сахароаминной реакции, которая протекает в четыре этапа. На каждом этапе образуются побочные продукты, чередующиеся хиноидными связями, затем они стабилизируются, превращаясь в ароматические и гетероциклические соединения.
Несмотря на то что до настоящего времени проведено много работ по изучению химического состава меланоидинов, до сих пор еще не установлена их химическая природа.
Меланоидины в виноделии, по мнению М. А. Герасимова (1951), имеют важное значение.
Крепким и десертным винам (кагору, мадере и токайским) меланоидины придают специфический вкус и аромат.
Отдельные аминокислоты и продукты деградации сахаров, участвующие в меланоидинообразовании, играют важную роль в формировании специфических тонов и оттенков аромата и вкуса.
В сахароаминной реакции участвуют продукты, возникающие в результате окислительного дезаминирования аминокислот и деградации сахаров в процессе нагревания. В. Л. Кретович и Р. Р. Токарева (1948) показали на модельных опытах, что когда в растворах присутствуют лейцин и валин, то образуются специфические тона «корки ржаного хлеба».
Таким образом, при меланоидиновой реакции образуются не только высокомолекулярные соединения — меланоидины, но и низкомолекулярные летучие вещества различного строения. Эти летучие вещества участвуют в формировании вкуса и букета вина.

