Следует прежде всего отметить, что при построении систем дыхания широко использованы каталитические механизмы, химические пути, а также принципиальные особенности ультраструктуры органоидов, молекулярной организации клеточных мембран, совокупностью которых обеспечивалось выполнение функции фотосинтеза. Многие из механизмов получили дальнейшее развитие, подвергались постепенному усложнению, совершенствованию.

Рис. 1. Цепь транспорта электронов при фотосинтезе (I) и дыхании (II)
Принципиальная же близость функций фотосинтеза и дыхания, „родимые пятна“, которые дыхание унаследовало от фотосинтеза, могут быть продемонстрированы на ряде очень наглядных примеров. Назовем, хотя бы, принципы -построения цепи транспорта электронов и природа осуществляющих эту функцию переносчиков (рис. 1). Особую роль при формировании ЭТЦ как фотосинтеза, так и дыхания сыграло то, что его основу составляло возможно большее удлинение цепи пробега мобилизованных электронов.
Этим обеспечиваются минимальные перепады энергии между соседствующими звеньями цепи. Таково важнейшее условие, которым обеспечивается способность клетки наиболее эффективно использовать энергию электронов.
По образному выражению Сент-Дьерди, живая клетка избегает больших потерь энергии главным образом потому, что она расплачивается мелкой монетой.
Об эволюционной связи дыхания и фотосинтеза свидетельствует близость, а в отдельных случаях и полная идентичность основных процессов биосинтеза углеводов в акте фотосинтеза, с одной стороны, и их окислительного распада — с другой. Идентична, наконец, природа весьма активных в биологическом отношении метаболитов, образующихся в качестве промежуточных продуктов как при фотосинтезе, так и в акте дыхания (активные пентозы, составляющие основу различных нуклеотидов, циклические и другие соединения и многие важные их производные).
Как уже указывалось, основу дыхания составляют процессы активирования и мобилизации водорода (электронов) субстрата, а также активирования молекулярного кислорода и процессов его восстановления. Тонкое отрегулированное взаимодействие осуществляющих эти процессы регуляторных механизмов и обеспечивает клетке способность эффективно использовать кислород в качестве конечного акцептора электронов.
Важным условием осуществления такого рода сопряжения явилась возможность возникновения специализированной категории морфологических структур-митохондрий. Ультраструктура этих образований и молекулярная организация их мембран обеспечивает высокую эффективность осуществляемых ими функций. Специфическая особенность последних состоит в том, что окисление служит здесь не только целям извлечения энергии субстрата и образования АТФ, но одновременно источником метаболитов, используемых клеткой в конструктивных целях.
Рассмотрим основные принципы организации каталитического аппарата, свойств составляющих его компонентов и путей, которыми регулируется способность растительной клетки вовлекать кислород в акт дыхания. При этом необходимо учитывать специфические особенности условий, в которых осуществляется дыхание у растений-организмов, лишенных стабильной внутренней среды (парциальное давление O2 и СO2, температура и др.).
Непостоянство, изменчивость этих факторов не могли не сказаться на ферментативных системах дыхания и, в первую очередь, естественно, на механизмах, осуществляющих заключительные его этапы, восстановление кислорода.
Три принципиальные особенности характеризуют структуру окислительного аппарата растений. Первой среди них следует считать то, что при построении окислительных систем у растений широко используется принцип множественности (мульти-принцип), в результате чего в растительной клетке мы встречаемся, как правило, не с одним, а с несколькими энзимами, катализирующими одни и те же или близкие по значению функции. Этим обусловлена характерная для окислительного аппарата растений динамичность, изменяемость соотношений, доли участия отдельных каталитических систем, альтернативность путей, которыми осуществляются процессы биологического окисления. Наличие альтернативных механизмов и путей окислительного обмена играет исключительно важную роль как фактор, расширяющий адаптивные, приспособительные возможности растения. Переключение этих механизмов обуславливает способность растений сохранять необходимый уровень и эффективность дыхательного процесса в непрерывно изменяющихся условиях внешней среды, включая различные экстремальные воздействия.
Второй весьма важной особенностью окислительного аппарата растений является большое место, которое в числе составляющих его компонентов занимают катализаторы, обладающие не одним, а несколькими свойствами (т. наз. полифункциональные системы).
Принципиальной особенностью окислительного аппарата следует считать, наконец, его рассредоточенность, делокализованность. Окислительными системами той или иной сложности и эффективности, как установлено, обладают практически все структурные компоненты протопласта. В этом отличие дыхательной функции от фотосинтеза, осуществлять который способны, как известно, только зеленые пластиды — хлоропласт.
Весьма важным этапом в развитии учения об энзиматической природе дыхания явилось открытие факта гетерогенности белковых компонентов различных окислительных ферментов. Для большинства этих компонентов характерно наличие того или иного числа молекулярных форм белка, различающихся по электрофоретической подвижности (величина и знак заряда), субстратной специфичности, кинетическим параметрам и ряду других свойств. Компоненты эти известны под именем изозимов или изоэнзимов.
Изозимные белки в определенных условиях (разбавление, воздействие детергентов, изменения pH) способны диссоциировать. При этом образуются т. наз. субъединицы. Последующая рессоциация субъединиц может сопровождаться образованием белка, каталитические свойства которого в том или ином отношении отличаются от исходного. Подобного рода явление имеет, например, место в инфицированной клетке, где происходит образование гибридных ферментов за счет субъединиц одноименных каталитических систем растения-хозяина и паразита.
Приведем некоторые примеры, иллюстрирующие воплощение перечисленных выше принципов структурной организации окислительного аппарата клетки.
В группе оксидазметаллопротеидов принцип полифункциональности отчетливо выражен на примере пероксидаз и фенолаз. Создавая модель полной системы биологического окисления, А. Н. Бах, как известно, считал пероксидазу необходимым, обязательным компонентом последней. В течение многих десятков лет эта идея не только не находила признания, но, по существу, нацело отрицалась.
В самые последние годы обстановка в этой области радикально изменилась. Трудно назвать фермент, который в настоящее время привлекал бы внимания больше и исследовался бы более углубленно, чем пероксидаза. Причиной все возрастающего внимания, которое привлекает пероксидаза, как раз и служит весьма характерная для этого фермента множественность форм и функций и весьма слабо выраженная субстратная специфичность. Известно, что свое название пероксидаза получила в связи с тем, что этот фермент, как предполагалось, способен взаимодействовать лишь с активированным перекисным кислородом. В настоящее же время установлено, что, наряду с этим, пероксидаза способна функционировать как типичная оксидаза, осуществляя окисление большого числа субстратов самой различной химической природы за счет свободного молекулярного кислорода. Важно, кроме того, что одно из используемых пероксидазой перекисных соединений — перекись водорода — образуется в клетке в ходе процесса окисления, осуществляемого ферментами флавиновой группы. В этом еще одно свидетельство существования прочной функциональной сопряженности пероксидазы со всеми другими звеньями процессов энергообмена растительной клетки. Все это и даёт основание рассматривать пероксидазу как один из полноценных альтернативных элементов окислительного аппарата клетки.
В структуре этой системы с большой отчетливостью воплощены все принципиальные особенности, характерные для дыхательных систем растения.
Столь же ярко эти принципиальные особенности выражены у одного из медьсодержащих протеидов, функции которого связаны с окислением фенолов О- и П-дифенолоксидазы. Эти ферменты также относятся к катализаторам со смешанными функциями, поскольку они способны катализировать одновременно две различные по механизму функции: окисление и гидроксилирование.
Субстратами фермента служит большое число различных фенолов и их производных. Вопрос о роли фенолазных ферментов в энергообмене живой клетки пока окончательно не решен.
Еще совсем недавно возможность какого-либо участия данной группы ферментов в нормальном дыхательном метаболизме отрицалась. Однако в последнее время установлено, что продукты окисления дифенолов — ортохиноны, могут в живой клетке восстанавливаться и таким путем выполнять роль промежуточных переносчиков электронов при окислении большого числа различных биологически важных соединений, как, например, аскорбиновая кислота, аминокислоты, восстановленные формы дегидрогеназ. Экспериментально показано участие фенолаз в окислении индолилуксусной кислоты. Эти данные служат убедительным доказательством правильности идей В. И. Палладина, сформулированных им свыше полувека тому назад.
Большой важности биологическая роль принадлежит системе фенолы — хиноны и регулирующие их превращения ферментных систем в реакциях фотоиммунитета.
Несколько слов о третьем звене перекисной теории Баха. Известно, что наряду с окислением дыхательного субстрата посредством активирования и отнятия водорода А. Н. Бах постулировал возможность прямого присоединения кислорода к субстрату, его непосредственного внедрения в молекулу последнего.
Доказать правильность этой идеи удалось лишь недавно путем применения тяжелого изотопа кислорода (18О), а также содержащей тяжелый кислород воды (Н2O18). Эти опыты позволили подтвердить одну из основных идей теории А. Н. Баха и вместе с тем открыли новую главу в учении о механизмах, катализирующих биологическое окисление.
Было открыто явление "фиксации кислорода", а ферменты, осуществляющие эту реакцию, именуются термином, предложенным А. Н. Бахом, "оксигеназы". В настоящее время имеются веские основания считать, Что прямое включение кислорода в органические молекулы представляет собой один из весьма широко распространенных механизмов биологического окисления. Итак, в отличие от других групп окислительных ферментов, оксигеназы катализируют непосредственное взаимодействие кислородных атомов не с водородом, а с атомами углерода ароматического кольца, которое подвергается при этом расщеплению. Биологическое значение реакций, катализируемых оксигеназами, заключается в основном в том, что осуществляемое ими гидроксилирование бедных кислородом ароматических соединений, а также стероидов и липидов повышает их растворимость и тем самым способствует включению этих соединений в метаболизм живой клетки. Функциональное действие оксигеназ самым тесным образом связано с системой ферментов, регулирующих превращения фенольных соединений.
Как отмечалось вначале, к числу основных принципов, использованных при построении окислительного аппарата живой клетки, относится его делокализация. Рассредоточенность биосинтетических функций, осуществляемых различными органоидами и относящихся к категории эндоэргонических, уже давно требовала выяснения вопроса об источниках потребляемой в ходе этих процессов энергии. Столь же существенное значение имеет этот вопрос для выявления путей восстановления кислорода, диффузно проникающего во все без исключения участки и структурные компоненты живой протоплазмы.
Основным, специализированным органоидом, генерирующим энергию, используемую при вторичных синтезах, служат, как известно, митохондрии. Одним из важных событий в учении об окислительном обмене живой клетки, имевших место в последние годы, явилось установление того факта, что наряду с митохондриями, автономными, генерирующими энергию системами той или иной степени сложности и эффективности обладают и другие структурные компоненты живой клетки. К их числу относятся, в частности, компоненты ядерной фракции, для которых экспериментально доказано, что они, кроме ферментов гликолитического (анаэробного) цикла, обладают системами, осуществляющими процессы окислительного фосфорилирования.
Достаточно полным набором окислительных ферментов обладают пластиды и, прежде всего, хлоропласт, компоненты микросомальной фракции и, наконец, растворимой фазы клетки. Системы транспорта электронов к кислороду у каждого из названных видов органоидов в значительной мере специфичны. Они различаются по степени сложности, природе отдельных компонентов и др. Различия эти, однако, не имеют принципиального значения. Хочется подчеркнуть, что в соответствии с теорией А. Н. Баха практически для всех органелл характерно наличие в системе ЭТЦ пероксидазы. Более подробного освещения требует вопрос об окислительных системах и функциях недавно обнаруженной категории органоидов, известных под именем пероксизом. Основанием для этого служит связь пероксизом с процессом фотодыхания, под которым имеется в виду зависимое от действия света поглощение кислорода, сочетающееся с выделением углекислого газа.
Явление фотодыхания установлено у большой группы высших растений и водорослей с высокой по СO2 компенсационной точкой (шпинат, подсолнечник, табак, пшеница, бобовые). У растений с низкой по СO2 компенсационной точкой это явление практически не обнаруживается (кукуруза, сахарный тростник, сорго и др.). Эти растения, как мы видели в первой части данной главы, относятся к группе С-4. Для ферментных систем пероксизом характерна очень высокая активность каталазы.
Одна из основных функций пероксизом связана с окислением гликолевой кислоты, которое осуществляет фермент гликолатоксидаза. Вместе с тем окисление гликолевой кислоты пероксизомам и представляет собой лишь одно из звеньев сложной цепи процессов, осуществляющихся с участием ферментных систем.
В пероксизомах происходит окисление гликолевой кислоты, образующейся в хлоропластах на свету. Продукт окисления — глиоксилевая кислота аминируется главным образом за счет глутамата при участии специфического фермента, в результате чего образуется аминокислота — глицин. Дальнейшие превращения глицина приводят к образованию серина, что осуществляется при одновременном декарбоксилировании одной из молекул глицина. Выделяющаяся при этом углекислота и является продуктом фотодыхания. Этот процесс сосредоточен в митохондриях (рис. 2).
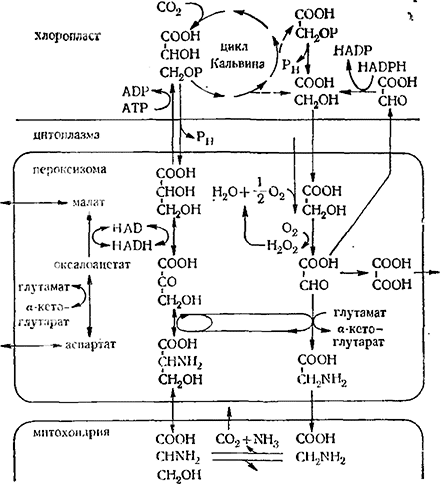
Рис. 2. Путь окислительных превращений гликолевой кислоты при фотодыхании
На примере фотодыхания демонстрируется принцип "кооперирования" функций различных морфологических структур клетки, участвующих в превращениях одного и того же химического соединения. В нем участвуют хлоропласты, пероксизомы, митохондрии, цитоплазма. Вместе с тем эта функция может служить еще одним примером тесной взаимосвязи столь противоположных на первый взгляд процессов, какими являются фотосинтез, в одной стороны, и дыхание — с другой.
Итак, живая клетка представляет собой орган, обладающий весьма многочисленной, гетерогенной в функциональном отношении системой окислительных и восстановительных энзиматических механизмов. Совокупность последних обеспечивает клетке возможность удовлетворять свои пластические и энергетические потребности за счет множества различных субстратов и осуществлять мобилизацию и транспорт электронов от последних к молекулярному кислороду различными путями.
Некоторое представление об арсенале средств, которыми наделена клетка для осуществления важнейшего акта, каким является терминальное окисление, можно получить из схемы (рис. 2).
Переключение альтернативных путей дыхания несомненно играет в жизни клетки важнейшую и притом разностороннюю роль. В ходе катализа, осуществляемого альтернативными системами, образуются различные промежуточные соединения (интермелиаты), активно включающиеся в общий метаболизм клетки. Они выполняют защитную роль против продуктов жизнедеятельности патогенных микроорганизмов в детоксикации чуждых организму соединений (гербицидов, пестицидов, дефолиантов и др.). Известная взаимозаменяемость отдельных окислительных систем должна иметь большое значение как средство адаптации организма, и, в частности, поддержания жизнеспособности при различного рода неблагоприятных воздействиях на организм (смена температуры среды, условия снабжения кислородом и др.).

