Билько Марина Владимировна, к.т.н., докторант, доцент,
Национальный университет пищевых технологий, Украина, г. Киев, ул. Владимирская 68;
Гержикова Виктория Григорьевна, д.т.н., профессор, главный научный сотрудник,
Ермихина Марианна Вадимовна, н.с. отдела химии и биохимии,
Зайцев Георгий Павлович, вед. инженер лаборатории аналитических исследований
«Национальный научно-исследовательский институт винограда и вина «Магарач»
АНТИОКСИДАНТЫ - ФАКТОРЫ ЗАЩИТЫ АНТОЦИАНОВ ОТ ОКИСЛЕНИЯ
В статье представлены результаты исследования массовой концентрации антоцианов модельных систем розовых виноматериалов при индуцированном окислении. Изучено влияние антиоксидантов (аскорбиновой кислоты, диоксида серы, восстановленного глутатиона, галлотанина) отдельно и в сочетании на содержание неокисленных форм антоцианов.
Установлено, что 70% всех антоцианов модельных систем розовых виноматериалов составляют мальвидин- гликозид и его ацетильные и n -кумароил производные, которые являются более стабильными к окислению, чем другие представители этого класса. Показано, что применение комбинации антиоксидантов на основе диоксида серы и восстановленного глутатиона позволяет защитить антоцианы модельных систем розовых виноматериалов от окисления и обеспечить сохранение их форм на уровне 92% исходного содержания.
Ключевые слова: розовые вина; ВЭЖХ; антоцианы; антиокислительный эффект; окисление.
Розовые вина разнообразием своих цветов и стилей обязаны антоцианам. В винограде и вине они представлены гликозидами мальвидина, дельфинидина, пеонидина, цианидина, которые различаются по своему строению: содержанию гидроксильных групп, присоединенных к молекуле углеводов, положению гликозилирования, количеству алифатических или ароматических кислот, связанных с сахарами. Следствием различного строения антоцианов в винах является их цвет на основе сочетания красных, синих и оранжевых оттенков [1-3].
Согласно литературным данным [2, 4-7], причиной снижения интенсивности цвета розовых вин, его трансформации в сторону абрикосово-оранжевых оттенков является совокупность химических реакций, протекающих в процессе приготовления виноматериалов данного типа. Так, взаимодействие антоцианов с танинами приводит к образованию стабильных антоциан-танинных комплексов, концентрация которых в розовых винах невелика и, следовательно, их роль в формировании цвета розовых вин не является главенствующей, как в случае красных вин [2]. Снижение концентрации антоцианов в процессе брожения обусловлено их частичной адсорбцией на клетках дрожжей и взаимодействием с ацетальдегидом [4]. В последние годы количество антиоксидантов, используемых в виноделии, растет, в научных публикациях встречаются исследования, связанные с использованием восстановленного глутатиона дрожжей [8, 9], препаратов танина [8, 10-12], аскорбиновой [8, 13, 14] и дегидроксифумаровой кислот [15]. Учитывая разный механизм защитного действия данных препаратов, можно предположить и их разную эффективность в отношении защиты антоцианов как основных факторов формирования цвета розовых вин.
В связи с этим целью настоящих исследований являлась оценка эффективности различных антиоксидантов в аспекте защиты антоцианов модельных систем, имитирующих розовые виноматериалы, от окисления.
Экспериментальные исследования осуществляли на модельных системах, представляющих собой водноспиртовые растворы с объемной долей спирта 10 %, подкисленные винной кислотой до рН 3 и содержащие танин кожицы винограда в концентрации 200 мг/дм3 и красящие вещества спиртовой вытяжки из кожицы винограда сортов Мерло и Пино нуар в концентрации 40 мг/дм3. Внесение препаратов антиоксидантов в модельные системы осуществляли в соответствии со схемами, представленными в табл.1. Выбор антиоксидантов и их дозировок был обоснован в результате проведенных ранее исследований [16-18].
Индуцированное окисление модельных систем осуществляли в термокамере при t=45±50C в течение 7 дней со свободным доступом воздуха. Температура была подобрана экспериментально с целью изучения способности модельных систем розовых виноматериалов развивать состояние окисленности во времени [16].
Таблица 1
Схема внесения антиоксидантов в модельные системы
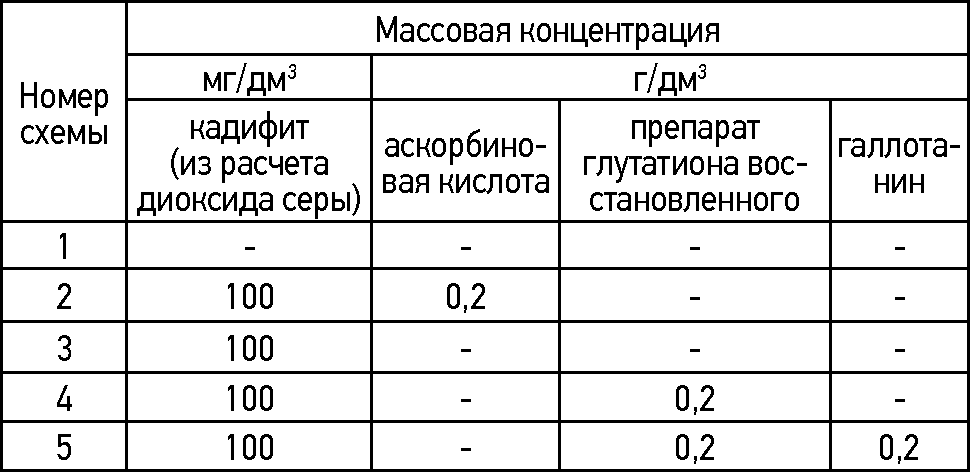

Рис. Влияние антиоксидантов на окисление антоцианов: схемы 1 - без защиты; 2-5 - с применением антиоксидантов: 2 - кадифита и аскорбиновой кислоты; 3 - кадифита; 4 - кадифита и восстановленного глутатиона; 5 - кадифита, восстановленного глутатиона и галлотанина
Определение массовой концентрации антоцианов до и после индуцированного окисления проводили методом ВЭЖХ [19]. Оценку защитного действия антиоксиданта оценивали по соотношению массовой концентрации антоцианов до и после индуцированного окисления и выражали в процентах от их исходного содержания.
Результаты исследования и их обсуждение.
Для сравнительной оценки склонности отдельных представителей антоцианов к окислению нами исследовался качественный состав и количественное содержание комплекса антоцианов полученной модельной системы. Результаты хроматографических исследований показали, что антоциановый комплекс представлен тремя группами антоцианов: I - гликозидами антоцианов, II - их ацетильными и III - n-кумароил производными. Преобладающими являлись гликозилированные формы антоцианов, доля которых в комплексе составляла 56-59%, тогда как ацетильные производные составляли 25-29%, а n-кумароил производные - 15-16%. Доминирующими в каждой из групп антоцианов были производные мальвидина, доля которых варьировала от 64 до 76%, что позволяет предположить их существенное влияние на формирование цвета модельной системы.
Проведение индуцированного окисления модельной системы в отсутствие антиоксидантов (схема 1) показало, что общая концентрация антоцианов после окисления снизилась на 43%, при этом концентрация гликозилированных форм снизилась на 42%, ацетилированных форм - на 41% и кумароил-производных - на 48% (рис.). Среди гликозилированных форм антоцианов наименее подвержены окислению гликозиды пеонидина и мальвидина, доля которых по окончании окисления составляла в среднем 64% от их исходной концентрации. Согласно литературным данным [2, 6, 20], это связано с отсутствием гидроксильных групп в орто-положении ядра В их молекул. Такую же высокую (в сравнении с другими производными антоцианов) устойчивость к окислению проявили и ацетилированные производные пеонидина, мальвидина и цианидина. Снижение их концентрации в ходе окисления составило 44, 40 и 33% соответственно, тогда как концентрация других антоцианов из этой группы в процессе индуцированного окисления снижалась на 63-66%. Среди кумароил-производных антоцианов наибольшее влияние индуцированное окисление оказало на дельфинидин. Его концентрация снизилась на 62%, тогда как других представителей этой группы - на 42-50%.
Сравнительный анализ эффективности защитного действия используемых антиоксидантов в отношении антоцианов показал следующее (табл. 2). Наиболее полному сохранению антоцианового комплекса в модельной системе способствовало совместное использование сульфитации и препаратов глутатиона восстановленного и галлотанина (схема 4 и 5). Низкий, в сравнении с другими приемами, антиокислительный эффект технологического приема, предусматривающего совместное использование диоксида серы и аскорбиновой кислоты (схема 2), скорее всего связан с тем, что образующийся в результате окисления аскорбиновой кислоты пероксид водорода инактивируется диоксидом серы, тем самым снижая его защитную функцию в отношении антоцианов [21].
Наряду с этим данные, представленные в табл. 2, показывают, что эффективность защитного действия антиоксиданта в пределах одной группы антоцианов значительно варьирует. Так, совместное использование диоксида серы и препарата глутатиона восстановленного (схема 4) способствовало наиболее полному сохранению гликозидов дельфинидина и пеонидина, а диоксида серы, препаратов глутатитона восстановленного и галлотанина (схема 5) - цианидина, петунидина и мальвидина.
Наиболее выраженный защитный эффект совместного использования глутатиона восстановленного и диоксида серы проявился в отношении кумароил-производных антоцианов, концентрация которых по окончании индуцированного окисления составляла от 87 до 100% от их исходной концентрации.
Таким образом, установлено, что наибольшим антиоксидантным эффектом в отношении антоцианового комплекса характеризовался технологический прием, предусматривающий совместное использование диоксида серы и препарата восстановленного глутатиона, использование которого способствовало сохранению антоцианов на 92 %.
Таблица 2
Рейтинг эффективности антиоксидантов в отношении антоцианов

СПИСОК ЛИТЕРАТУРЫ
- Moreno-Arribas, М. V. Wine Chemistry and Biochemistry / М. V. Moreno- Arribas, C. Polo - New York: Springer, 2009. - 736 p.
- Handbook of Enology. The Chemistry of Wine Stabilization and Treatments / P. Rib'ereau-Gayon, Y. Glories, A. Maujean, D. Dubourdieu. - [2nd Edition] - John Wiley & Sons, 2006. - 441 р.
- Функции и свойства антоцианов растительного сырья / А.М. Макаревич, А.Г. Шутова, Е.В.Спиридович, В.Н.Решетников //Труды БГУ. - 2010. -Т.4, в. 2. -С.1-11.
- Escudero-Gilete, M.L. Implications of blending wines on the relationships between the colour and the anthocyanic composition /M.L.Escudero-Gilete, M.L. Gonzalez-Miret, F.J.Heredia //Food Research International. - 2010. - №43. - P.745-752.
- Bisca, Vasilina. Cercetarea si elaborarea tehnologiei vinurilor roze cu indici cromatici stabili. Autoreferat al tezei de doctor in tehnica: 05.18.07“Tehnologia bauturilor alcoolice §inealcoolice” / V. Bisca. - Chisinau, 2008. - 28 с.
- Wrolstada, Ronald E. Tracking color and pigment changes in anthocyanin products / Ronald E. Wrolstada, Robert W. Dursta, Jungmin Lee // Trends in Food Science & Technology. - 2005. - № 16. - p. 423-428.
- Nuancier papier adapts a la couleur des vins de Provence [Электронный ресурс] / Centre du Rose // Informations Techniques - 2010. - №1. - С. 1. - Режим доступа: http://www.centredurose.fr/info%20vins%20roses/
- Ткаченко, О. Б. Научные основы совершенствования технологии белых столовых вин путем регулирования окислительно-восстановительных процессов их производства: дис докт. техн. наук: 05.18.05 «Технология сахаристых веществ и продуктов брожения» / О.Б. Ткаченко. Национальный институт винограда и вина «Магарач». - Ялта, 2010. - 340 с.
- Toit, Wesssel. Effect of different oxygen levels on glutathione levels in South African white must and wines [Электронный ресурс] / Wessel du Toit, Klemen Lisjak. Режим gocmyna:http://www.bucher-inertys.com/web/upload_fich/ effect_of_different_oxygen_levels.pdf
- Scollary, G. R. Tannin Review / Dr Geoffrey R Scollary. - Melbourne, 2010. - 132p.
- Obradovic, D. Grape-derived tannins and their application / D. Obradovic // Australian & New Zealand Grapegrower & Winemaker. - 2006. - № 509. - р. 66-73.
- Improving color extraction and stability in red wines: the use of maceration enzymes and enological tannins / A. B. Bautista-Ortin, A. Martinez-Cutillas, J. M. Ros-Garcia [et al] // International Journal of Food Science & Technology. - 2005. - Vol. 40, №4. - Р. 867 - 878.
- Barril, C. Chemistry of sulfur dioxide and ascorbic acid as an anti-oxidant system in white wine / C. Barril, A. C. Clark, G. R. Scollary // National Wine and Grape Industry Centre, Charles Sturt University. - 13 April 2010. - 140 p.
- Беглица, В. М. Усовершенствованная технология производства розовых столовых вин: автореф. дис канд. техн. наук : спец. 05.18.07 «Технология продуктов брожения, алкогольных и безалкогольных напитков» / В.М. Бегли- ца. - Ялта, 1989. - 24 с.
- Гонца, М. Окислительно-восстановительные процессы в винах и стабилизация с использованием новых консервантов [Электронный ресурс] / М. Гонца // Режим доступа: http://iee.org.ua/files/conf/conf_article55.pdf
- Управлiння окисно-вiдновними процесами при виробництвi рожевих столових виномaтерiaлiв / М. В. Бiлько, А. I. Тенетка, М. В. Скорченко, I. М. Бабич// Hayковi працi ОНАПТ. - 2012. - № 42, т. 2. - С. 330-335.
- Бiлько, М. В. Деяк аспекти формування фенольного комплексу рожевих столових виномaтерiaлiв / М. В. Бiлько, А. I. Тенетка // Напитки. Технологии и инновации. - 2012. - №4. - С. 56-59.
- Bilko, M. The regulation doses of sulfur dioxide with the aid of preparations, based on glutathione of yeasts in the production of pink table wine / M. Bilko, A. Tenetka // Ukraine journal of food science. - 2013. - №1. - p. 77-82.
- Ульянова, Е.В. Высокоэффективная жидкостная хроматография в исследовании антиоксидантных свойств вин / Е.В. Ульянова, О.Г. Ларионов, А.А. Ревина // Сорбционные и хроматографические процессы. - 2010. - Т.10. Вып. 4. - С. 522-532.
- Jackson, R. Wine Science. Principles and Applications / Ronald S. Jackson - Elsevier, 2008. - 752 p.
- Clark, A. C. Chemistry of sulfur dioxide and ascorbic acid as an anti-oxidant system in white wine / Dr Andrew C Clark. - Melbourne, 2010. - 56 p.

