Масс-спектрометрия стабильных изотопов кислорода 18О/16О в винодельческой продукции для установления ее подлинности
А.Ю. КОЛЕСНОВ, д-р техн. наук, канд. биол. наук; И.А. ФИЛАТОВА, канд. техн. наук;
Д.Г. ЗАДОРОЖНЯЯ, канд. техн. наук; О.А. МАЛОШИЦКАЯ, канд. хим. наук
ФГБОУ ВПО «Московский государственный университет пищевых производств»
Ключевые слова: стабильные изотопы, кислород, масс-спектрометрия, винодельческая продукция, идентификация, подлинность, фальсификация Keywords: stableisotopes, oxygen18О/16О, mass-spectrometry, wineproducts, identification, authenticity, adulteration
Введение.
Позитивные аспекты объединения рынков (ЕврАзЭС, Таможенный союз, ВТО), в том числе расширение ассортимента, увеличение конкурентной борьбы за доверие потребителей и, как следствие, улучшение конкурентоспособности продукции, сопровождаются также определенными негативными моментами (усиление тенденций использования недобросовестных способов ведения конкурентной борьбы, к наиболее распространенным из которых относится фальсификация* продукции, в том числе снижение ее себестоимости за счет манипуляций с составом). К определенным недостаткам, препятствующим улучшению конкурентоспособности пищевой продукции, можно отнести изолированность российского рынка, которая может быть использована отдельными участниками для получения экономических преимуществ за счет ограничения конкуренции извне и снижения законодательных и нормативных требований к качеству и безопасности продукции [1].
Повышение конкурентоспособности продукции и защита российских участников рынка и, не в последнюю очередь потребителей, за счет повышения уровня к качеству и безопасности продукции могут быть достигнуты только в результате применения комплекса мер, в котором неотъемлемой составляющей является полная, а не частичная гармонизация нормативных требований с международными. Кроме того, особую роль и значение приобретают разработки пищевой науки, одной из главных задач которой становится обеспечение участников российского рынка, в особенности из сферы оценки соответствия, новыми современными методологиями исследования компонентного состава продовольственного сырья, пищевых продуктов и добавок, ароматизаторов, технологических и вспомогательных средств, направленными на предотвращение или минимизацию современных техногенных, биогенных и антропогенных рисков и угроз качеству и безопасности продукции, создание и поддержание условий добросовестной конкуренции, защиту интересов потребителей, изготовителей и поставщиков высококачественных, подлинных и безопасных продуктов. Именно комплексный подход позволит обеспечить общественное доверие к продукции, представленной на российском рынке, в особенности в условиях ЕврАзЭС, Таможенного союза и ВТО.
Цель и задача научно-исследовательской работы. Основная цель исследовательских работ, проводимых в ФГБОУ ВПО «МГУПП», — современное научное обеспечение мероприятий по реализации положений «Доктрины продовольственной безопасности», положений законодательных и нормативных документов, «Стратегии развития пищевой и перерабатывающей промышленности Российской Федерации на период до 2020 года» (утверждена Распоряжением Правительства Российской Федерации от 17.04.2012 г. №559-р), направленных на повышение конкурентоспособности отечественных продуктов, создание и поддержание условий добросовестной конкуренции, защиту интересов потребителей, изготовителей и поставщиков высококачественной, подлинной и безопасной продукции. При этом научное обеспечение осуществляется.
путем разработки и внедрения новых методологий для практического исследования аспектов качества и безопасности пищевой продукции;
на основе прикладных научно- исследовательских работ по изучению состояния российского рынка пищевой продукции в сфере ее качества и безопасности;
в рамках консультационной и экспертной поддержки участников российского рынка пищевых продуктов;
путем внедрения результатов научных разработок в форме стандартов, сводов правил в практику оценки соответствия пищевой продукции.
Задача настоящего исследования, обеспечивающая достижение поставленной цели, состоит в создании методологических и инструментальных предпосылок для внедрения в практику достижений пищевой науки — результатов фундаментальных научно-исследовательских работ, проводимых в ФГБОУ ВПО «МГУПП», а также апробация и использование разработок для изучения качества и безопасности продукции в рамках научного мониторинга пищевого рынка.
Объект исследования — качество пищевой продукции. К предмету исследования относится изучение одного из главных критериев качества виноградных вин и виноматериалов — подлинности, которая с учетом происхождения, совокупности биологических и физико-химических свойств выбранных продуктов характеризуется особенностями распределения стабильных изотопов легких элементов, входящих в состав внутриклеточной воды, клеточной ткани и компонентов — химических соединений, определяющих характеристики матрицы пищевого продукта. Тема настоящего исследования — изучение состава стабильных изотопов кислорода 18О/16О в воде пищевых продуктов, представленных в розничной торговой сети под заявленным наименованием «Вино».
Материалы и методы.
Прикладную научно-исследовательскую работу проводили с использованием уникального автоматизированного аналитического комплекса, созданного в Лаборатории фундаментальных и прикладных исследований качества и технологий пищевых продуктов ФГБОУ ВПО «МГУПП» для проведения научных работ и практической апробации их результатов (рис. 1) и включающего:
систему подготовки проб к исследованию (Thermo Fisher Scientific, Германия), состоящую из термостатируемого штатива, прецизионного регулятора температуры, автоматического податчика проб GC PAL (СТС Analytics AG, Швейцария) с роботизированным манипулятором с универсальным двухпортовым игольчатым рабочим органом для подачи продувочной газовой смеси, отбора объемов газовой фазы и ее подачи в прибор управления;
прибор очистки и подачи проб Gasbench II (Thermo Fisher Scientific, Германия), состоящий из необслуживаемой диффузионной системы удаления воды из пробы на основе мембран Nafion, системы инжекции проб, изотермического газового хроматографа, активного интерфейса для деления газовых потоков и системы инжекции газов, используемых в качестве рабочих стандартов;
IRMS/SIRA2 изотопный масс- спектрометр Delta V Advantage (Thermo Fisher Scientific, Германия);
систему подачи газов высокой степени очистки «Сигм-Плюс» (ООО «Сигм-Плюс», Россия);
специализированную рабочую станцию Optiplex 960 (Dell, США) для регистрации и обработки экспериментальных данных на основе программного пакета высокого уровня Isodat 3.0 (Thermo Fisher Scientific, Германия).

Рис. 1. Автоматизированный аналитический комплекс для исследования стабильных изотопов легких элементов в Лаборатории фундаментальных и прикладных исследований качества и технологий пищевых продуктов ФГБОУ ВПО «МГУПП»
В исследовании пользовались международными стандартными образцами (МСО) с известным составом изотопов кислорода 18О/16О: «Международный стандартный образец среднеокеанической воды VSMOW2» (Vienna-Standard Mean Ocean Water 2, δ18Ο = 0,00 %o, МАГАТЭ3, Австрия), «Международный стандартный образец водных осадков ледяного покрова Гренландии GISP» (Greenland Ice Sheet Precipitation, δ18Ο = -24,76 %o, МАГАТЭ, Австрия) и «Международный стандартный образец легких водных осадков Антарктики SLAP2» (Standard Light Antarctic Precipitation 2, δ18Ο = -55,50 %o, МАГАТЭ, Австрия). Рабочим стандартным образцом (РСО) в исследовании служил углекислый газ высокой степени очистки 99,9999 %; продувочный газ — гелий высокой степени очистки 99,9999%, содержащий 0,5 % высокоочищенного углекислого газа; газ-носитель — гелий высокой степени очистки (все газы — ОАО «Линде Газ Рус», Россия).
Подготовка и очистка проб.
Принцип подготовки проб к исследованию определяют физические процессы термодинамического фракционирования (распределения) изотопов в природных системах (биотических и абиотических объектах). Постоянный обмен изотопами кислорода в природе происходит между жидкой и газовой фазами в процессе испарения воды. Интенсивность обмена является функцией времени, температуры и количества участвующих в обмене изотопов. В закрытых системах с течением времени интенсивность обмена снижается до наступления определенного равновесного состояния, в котором скорости перехода изотопов одного элемента из жидкой в газовую фазу и обратно равны. Данное состояние называется изотопным равновесием системы.
1 МАГАТЭ — Международное агентство по атомной энергии (г. Вена, Австрия).
IRMS/SIRA — Isotope Ratio Mass Spectrometry/Stable Isotope Ratio Analysis (масс- спектрометрия изотопных соотношений/анализ соотношений стабильных изотопов).
Методология, используемая для подготовки проб к исследованию изотопов кислорода и основанная на данном физическом явлении, получила название методологии изотопного уравновешивания.
Изотопный обмен до наступления равновесного состояния для закрытых систем, контролируемых по составу газовой фазы, температуре и длительности процесса, может быть представлен в виде общего уравнения:

Согласно общему уравнению, изотопный обмен происходит между молекулами углекислого газа, которые содержатся в закрытом объеме контролируемой газовой среды, и молекулами воды, в том числе молекулами воды, входящей в состав исследуемого жидкого объекта. Так, в закрытой системе один атом кислорода с атомной массой 16 из молекулы углекислого газа с массой 44 при взаимодействии в газовой фазе с молекулами воды замещается на один атом кислорода с атомной массой 18 с увеличением массы молекулы углекислого газа до 46 единиц. Измерение молекул углекислого газа с массами 44 и 46 позволяет определить количество изотопов кислорода 18О и 16О и рассчитать значение показателя ![]() для исследуемой пробы, содержащей воду.
для исследуемой пробы, содержащей воду.
Для проведения реакции изотопного уравновешивания исследуемые пробы объемом 0,200 мл (для воды) и 0,500 мл (для вина/виноматериалов) вносили в круглодонные пробирки из боросиликатного стекла объемом 12 мл. Пробирки герметично укупоривали одноразовой винтовой пробкой с тефлон-силиконовой мембраной. В аналогичные пробирки отдельно вносили МСО воды VSMOW2, GISP и SLAP2.
Для проведения исследований формировали серию, в которую входили необходимое количество пробирок с внесенными пробами и пробирки с МСО. Дополнительно в каждую серию включали пустую укупоренную пробирку (для контроля газовой смеси, используемой для замены воздушной атмосферы) и пробирки с внутренним лабораторным образцом (ВЛО) — бидистиллированной водой, полученной в Лаборатории фундаментальных и прикладных исследований качества и технологий пищевых продуктов ФГБОУ ВПО «МГУПП» с помощью бидистиллятора GFL 2104 (GFL, Германия).
Серию пробирок размещали в ячейках термостатируемого штатива прибора для подготовки проб. Как правило, в первых и последних ячейках штатива с целью контроля дрифта показаний размещали пробирки с МСО и ВЛО. Для проведения реакции изотопного уравновешивания воздушную атмосферу внутри пробирок заменяли инертным газом — гелием, содержащим 0,5 % РСО. Скорость потока газовой смеси до полного вытеснения атмосферного воздуха и создания в каждой пробирке контролируемой газовой среды определили экспериментальным путем: она составила 130 мл/мин при длительности замены 10 мин. Результаты предварительных экспериментов по установлению длительности реакции изотопного уравновешивания показывают, что равновесное состояние в созданной закрытой системе наступает после выдержки образцов в течение не менее 18 ч. При этом оптимальной температурой для проведения реакции определена температура 25±0,1 °C. Коэффициент разделения изотопов кислорода между углекислым газом и водой при данной температуре равен 1,0412 [2].
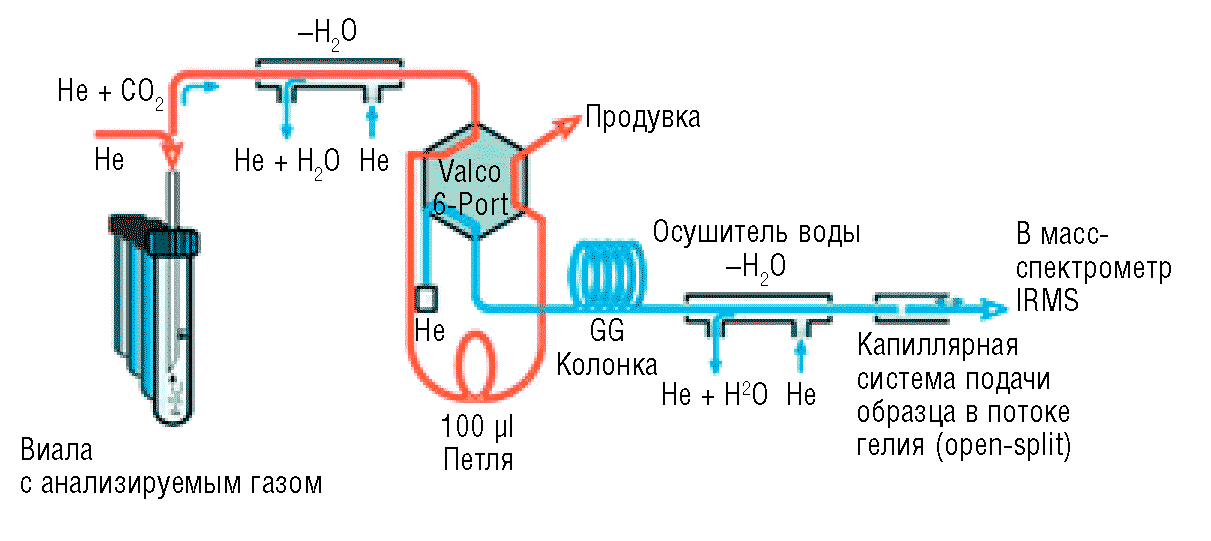
Рис. 2. Общая принципиальная схема основных этапов исследования изотопов кислорода в жидких пищевых продуктах в методологии изотопного уравновешивания
Температурный фактор — один из основных факторов влияния на результат изотопного обмена. Для обеспечения стабильности температурного режима на протяжении всей реакции важным требованием является активное поддержание установленного уровня температуры, которое достигается не только применением прецизионных устройств, но и регулируемым понижением и сохранением температуры в помещении, где размещено аналитическое оборудование, на 5...10 °C ниже температуры реакции изотопного обмена.
Измерение изотопов.
По окончании реакции изотопного обмена на следующем этапе предусмотрен отбор из газовой фазы каждой пробирки объемов газовой смеси, подаваемой в прибор Gasbench II. Газовую смесь, содержащую углекислый газ с равновесным изотопным составом атомов кислорода, подвергают первичной очистке с целью удаления молекул воды с помощью диффузионной системы на основе молекулярного мембранного сита Nafion, после чего направляют в систему газового хроматографа для выделения углекислого газа. Хроматографическое разделение газовых фракций осуществляют в потоке гелия (2 мл/мин) на колонке типа PLOT Fused Silica с неподвижной фазой марки СР- PoraPLOT Q, длиной 25 м и диаметром 0,32 мм (Varian, США).

Рис. 3. Типичный цифровой и графический модуль регистрации и обработки данных исследования стабильных изотопов кислорода 180 и 160 в в жидких пищевых продуктах
Температура хроматографического разделения газов составляла 70 °C, в то время как температура проб в штативе до окончания исследования поддерживалась на уровне 25+0,1 °C. Прибор Gasbench II позволяет в процессе одного цикла измерения осуществлять многократную подачу газовой смеси из системы инжекции в хроматограф. Одна инжекция газовой смеси означает одно хроматографическое разделение и, соответственно, одно измерение количественного соотношения изотопов кислорода 18О и 16О в изотопном масс-спектрометре Delta V Advantage. Перед подачей очищенных объемов углекислого газа в масс-спектрометр они подвергаются дополнительной обработке в диффузионной системе Nafion для удаления возможного загрязнения газовой фракции молекулами воды.
Для количественного измерения состава изотопов кислорода 18О и 16О подготовленные объемы углекислого газа направляют в масс- спектрометр Delta V Advantage. Значение ускоряющего напряжения масс-спектрометра составляет 3,07 кВ, рабочее давление в ионном источнике — 1,2· 10"7 кПа. Генерацию ионизированных молекул углекислого газа осуществляли способом электронного удара (уровень энергии электронов составил 124 эВ). Изотопный масс- спектрометр Delta V Advantage оснащен 5 детекторами — ионными ловушками (чашки Фарадея), три из которых осуществляют одновременный непрерывный мониторинг сигнала [СО2]+ для трех основных ионов с массами 44 (12С16О16О), 45 (13С16О16О и 12С17О16О) и 46 (12С16о18О). Для обеспечения значимого уровня сигнала резисторы отклика были настроены на значения 3-108, 3-1010 и 1-1011 Ом соответственно для масс 44, 45 и 46. В начале измерительного цикла в масс-спектрометр подавали по 5 объемов РСО.
Регистрировали, обрабатывали результаты исследований, а также управляли всеми приборами научного комплекса с помощью специализированной компьютерной рабочей станции Dell Optiplex 960 и программного пакета высокого уровня Isodat 3.0. Общая принципиальная схема основных этапов исследования изотопов кислорода в жидких пищевых продуктах методом изотопного уравновешивания представлена на рис. 2, типичный цифровой и графический модуль регистрации и обработки данных изотопного исследования — на рис. 3.
Результаты исследования. В настоящей публикации представлены результаты исследования 18 образцов вин из розничной сети Москвы и Московской области (см. таблицу). В торговых организациях розничной сети на продукцию, закупленную для проведения исследований, имелись документы, подтверждающие ее соответствие (сертификаты, декларации соответствия, свидетельства о государственной регистрации) нормативным требованиям. Из данных документов следовало также, что продукция соответствует заявленному наименованию.
Каждый образец исследовали согласно разработанной методологии в 5 повторностях. Значения стандартного отклонения в каждой серии определений не превысили уровня 0,200 %о.
Значения показателя 518О (%о) рассчитывали непосредственно в процессе регистрации и обработки данных программным пакетом Isodat 3.0. В основе расчета лежит следующая формула:
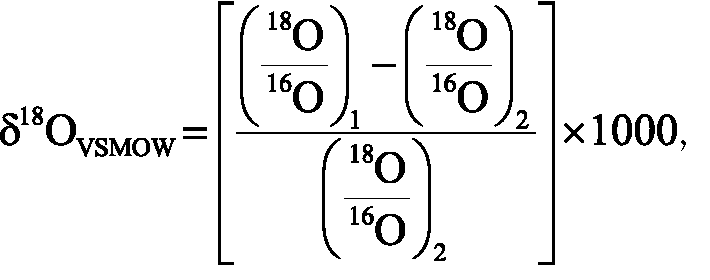
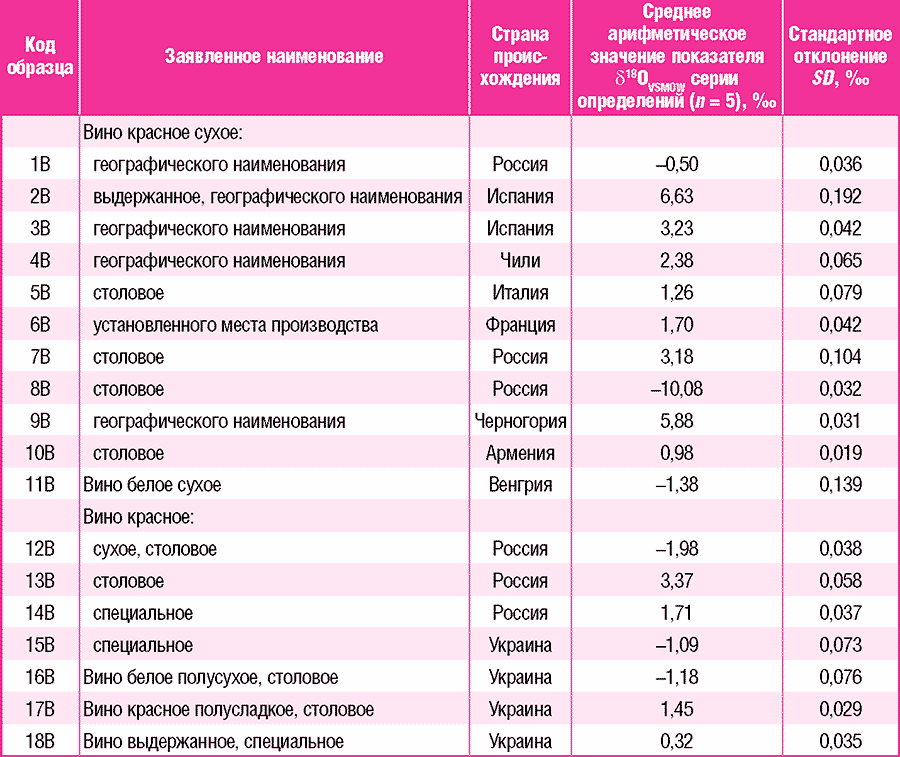
Примечание. SD— Standard Deviation.
где![]() — соотношение изотопов кислорода в пробе;
— соотношение изотопов кислорода в пробе;![]()
соотношение изотопов кислорода в стандартном образце.
В расчете использовали измеренные значения интенсивности сигналов молекул углекислого газа с массами 46 и 44. Для контроля правильности результатов важным аспектом служило проведение одновременной коррекции значений интенсивности сигнала для исключения возможного влияния изобаров![]() доля которых определяется по активности сигнала по массе 45 с учетом степени распределения изотопов 13С и 17О в природе (соответственно 1,11 и 0,0375%).
доля которых определяется по активности сигнала по массе 45 с учетом степени распределения изотопов 13С и 17О в природе (соответственно 1,11 и 0,0375%).
С учетом особенностей методологии изотопного уравновешивания и инструментальных решений, применяемых для ее реализации в измерительной системе Gasbench II (Thermo Fisher Scientific), значения показателя![]() (%о),
(%о),
рассчитываемые по результатам зарегистрированных сигналов по массам 44 и 46, дополнительно корректируют (нормализуют) с применением линейной зависимости между значениями показателя δ18О используемых МСО (VSMOW2, GISP, SLAP2), которые установлены в МАГАТЭ, и значениями, измеренными для указанных МСО, в каждой серии образцов. Пример типичной линейной зависимости между указанными параметрами, определенной в эксперименте, описывается уравнением у = 0,9764х — 27,128 (r = 0,99999962, r2 = 0,99999924). При этом коэффициент детерминации (г2) установленной линейной зависимости не должен быть менее 0,99999. В противном случае измерение для конкретной серии образцов, включая измерения МСО, входящих в данную серию, повторяют до выполнения указанного условия.
- Под биологической водой понимается внутриклеточная вода растительных объектов, специфичный изотопный состав которой определяет характер процессов метаболизма и водного обмена с окружающей средой, протекающих в растениях. Уникальной особенностью водного обмена, получившей название биологического изотопного эффекта, является обогащение высшими растениями внутриклеточной воды «тяжелым» изотопом кислорода 18О в ходе своего биологического развития.
- Под геологической водой понимается вода природных или искусственно созданных подземных или поверхностных объектов, используемых для промышленных целей в качестве источников питьевой и технологической воды, а также в целях снабжения населения питьевой водой. Специфичный уровень распределения изотопов кислорода в геологической воде определяют физические процессы (термодинамического и/или кинетического характера), протекающие в природных водных объектах, включая атмосферные процессы, связанные с испарением и выпадением водных осадков. Согласно базе данных GNIP/GNIR/WISER МАГАТЭ, а также результатам собственных исследований Лаборатории фундаментальных и прикладных исследований качества и технологий пищевых продуктов ФГБОУ ВПО «МГУПП» средние значения для геологической воды для основных географических регионов Российской Федерации, в которых выращиваются и перерабатываются фрукты, лежат в интервале от-11 до -14 %о.
Нормализованные значения показателя δ18Ο применяют при интерпретации результатов и составлении выводов исследования.
Выводы.
Результаты прикладной научно-исследовательской работы, проведенной в Лаборатории фундаментальных и прикладных исследований качества и технологий пищевых продуктов ФГБОУ ВПО «МГУПП» показывают, что в розничной торговой сети Москвы и Московской области присутствует винодельческая продукция, не соответствующая заявленному наименованию. Так, состав стабильных изотопов кислорода в образце 8В не совпадает с природным составом биологической воды4 винограда и, соответственно, натуральной (подлинной) винодельческой продукции. Согласно опубликованным данным минимальные значения показателя ![]() во внутриклеточной воде винограда и подлинных продуктах его переработки (например, виноградных соков, сусла, натуральных виноградных вин и других продуктов переработки винограда) не опускаются ниже границы -3 %о [3-8]. Существенные снижения показателя
во внутриклеточной воде винограда и подлинных продуктах его переработки (например, виноградных соков, сусла, натуральных виноградных вин и других продуктов переработки винограда) не опускаются ниже границы -3 %о [3-8]. Существенные снижения показателя![]() (например, в образце 8В) свидетельствуют об использовании в производстве геологической (питьевой) воды5. Доля фальсифицированной продукции в группе «Вино виноградное» в исследованной выборке продуктов составила 5,6 %.
(например, в образце 8В) свидетельствуют об использовании в производстве геологической (питьевой) воды5. Доля фальсифицированной продукции в группе «Вино виноградное» в исследованной выборке продуктов составила 5,6 %.
Общий результат проведенного прикладного научного исследования — выявление продукции, не соответствующей заявленному наименованию. Это позволяет обосновать вывод о необходимости совершенствования и корректировки системы оценки соответствия винодельческой продукции, в том числе путем внедрения и применения современных научных методологий для ее идентификации, исследования качества и безопасности. Данное совершенствование системы приобретает особую актуальность и значимость в связи с созданием единого экономического пространства в рамках ЕврАзЭС (Таможенного союза) и вступлением России в ВТО.
Дополнительные аспекты изотопных исследований. В работах, цель которых — изучение отдельных изотопных эффектов и определение соотношения между количествами интересуемых изотопов одного элемента, одним из аспектов является оценка массового баланса протекающих реакций и, соответственно, расчет количества компонентов, участвующих в данных реакциях. Так, в методологии изотопного уравновешивания значение имеют объем газа и, в особенности, количество пробы, содержащей воду, т. к. окончательный результат исследования (значение показателя δ18Ο) будет зависеть от состава исследуемых изотопов газа и пробы.
В исследовании согласно описанной выше методологии используется проба, содержащая воду и газы высокой степени очистки. Известно, что 1 М воды эквивалентен объему 18 мл, а 1 М идеального газа — 22,4 л. Объем пробирок (см. выше), в которых протекает реакция изотопного уравновешивания, составляет 12 мл. Данный объем эквивалентен 0,0005357 М идеального газа. Гелий, содержащий 0,5 % углекислого газа, в методологии изотопного уравновешивания рассматривается как идеальный газ. Таким образом, количество углекислого газа в объеме пробирки (12 мл) составит 0,000002679 М. Объем воды, равный, например, 1 мл, соответствует 1/18 М. При использовании данного объема концентрация атомов кислорода в водной фазе пробы в 10000 раз будет превышать концентрацию атомов кислорода в газовой фазе. Этого количества будет более чем достаточно для инициирования изотопной реакции и поддержания ее скорости вплоть до равновесного состояния, которое в конечном итоге обеспечивает эквивалентность изотопного состава жидкой и газовой фаз.
Таким образом, в реакции изотопного обмена, для реализации которой используется 1 мл или даже от 0,200 (в случае пробы, не содержащей растворенных сухих веществ) до 0,500 (с растворенными сухими веществами) мл жидкой пробы, расчет массового баланса не является обязательным. В проведенном исследовании использовали объемы 0,200 мл (для воды) и 0,500 мл (для вина) [9].
СПИСОК ЛИТЕРАТУРЫ
- Барсукова С.Ю. Патриотизм или прагматизм? Стратегии участников продовольственных рынков в России/С. Ю. Бapcyковa//Journal of Institutional Studies (Журнал институциональных исследований). 2010. Т. 2. №4. С. 84-105.
- Фор Г. Основы изотопной геологии/Г. Фор //М.: Мир, 1989. С. 445-475, 507-528.
- Свод правил для оценки качества фруктовых и овощных соков Европейской ассоциации фруктовых соков (Code of practice Al J N). M.: Нововита, 2004 (изд. на русском языке), 2008-2011 (дополнения на английском языке).
- Christoph, N. Possibilities and limitations of wine authentication using stable isotope and meteorological data, data banks and statistical tests. Part 1: Wines from Franconia and Lake Constance 1992 to 2001/N. Christoph, A. Rossmann, S. Voerkelius//Mitteilungen Klosterneuburg, 2003. 53. S. 23-40.
- Christoph, N. Possibilities and limitations of wine authentication using stable isotope ratio analysis and traceability. Part 2: Wines from Hungary, Croatia, and another European countries/N. Christoph, G. Baratossy, V. Kubanovic, B. Kozina, A. Rossmann, C. Schlicht, S. Voerkelius//Mitteilungen Klosterneuburg, 2004. 54. S. 144-158.
- Wachter, H. Verifying authenticity of wine by Mahalanobis distance and hypothesis testing of stable isotope pattern — a case study using the EU wine databank/H. Wachter, N. Christoph, S. Seifert//Mitteilungen Klosterneuburg, 2009. 59. S. 237-249.
- Camin, F. Control of wine vinegar authenticity through δ180 analysis/F. Camin, L. Bontempo, M. Perini, A. Tonon, 0. Breas, C. Guillou, J.M. Moreno-Rojas//Food Control, 2013 29 (1). P. 107-111.
- Kelly, S. Tracing the geographical origin of food: the application of multi-element and multi-isotope analysis/S. Kelly, K. Heaton, J. Hoogewerff// Trends in Food Science & Technology, 2005. 16 (12). P. 555-567.
- Gasbench II. Operating manual. Thermo Fisher Scientific/Gasbench II. Revision A-1118343, 2009. P. 5-33, 5-39, 5-42.

