Циркуляр от 16 августа 1956 г. Министерства сельского хозяйства Франции разрешил применять способ, позволяющий избежать осаждения винного камня в винах, не предназначенных для длительного хранения. Этот способ заключается в добавлении на каждый гектолитр обрабатываемого вина максимум 10 г метавинной кислоты, получаемой при разложении винной кислоты, нагретой до 170°С (точка плавления).
Когда нагревают кристаллы винной кислоты, измельченные в мелкозернистый порошок, в капсуле непосредственно над источником тепла или в термостате, то наблюдают плавление кристаллов при 170°С и нормальном давлении и при 150°С, если опыт ведут при пониженном давлении. Эта разница объясняется разложением молекулы винной кислоты, которое происходит при нагревании и которое будет рассмотрено ниже. Под вакуумом вода при дегидратации удаляется лучше. В результате получают бесцветную, относительно текучую жидкость. Если продолжать нагревание, несколько превышая указанные температуры, жидкость начинает бурно кипеть. Кипение сопровождается загустеванием, за которым быстро следует образование обильной пены, вызываемое значительным выделением газов. Сначала масса окрашивается в светло-желтый цвет, затем быстро, если температура остается высокой, в коричневый цвет. Под вакуумом окраска всегда остается намного более светлой.
Если нагревание прекратить в первой фазе (до кипения и появления пены), то при охлаждении получается стекловидная масса аморфной структуры, трудно поддающаяся дроблению, почти прозрачная, если плавление было кратковременным, или же матовая, непросвечивающаяся при более длительном плавлении. Если охлаждение наступает позднее (после образования пены), получают прочное вещество губчатой структуры, легкое по внешнему виду, похожее на хлебный мякиш, более или менее окрашенное в зависимости от интенсивности и продолжительности нагревания. Это вещество, т. е. метавинная кислота, легко дробится и превращается в порошок.
Первые исследования по плавлению винной кислоты
Реакции, которые происходят при нагревании винной кислоты, сложны. Механизм этих реакций был описан в работах, публиковавшихся еще с 1838 г., таких авторов, как Фреми, Браконо, Эрдман, Лораи и Герхардт, Пастер, Юнгфляйш, Десэнь, Шифф и др. Документацию по этим работам можно найти в «Химическом словаре» Вурца (1878). Механизм разложения винной кислоты, описанный этими авторами, можно резюмировать следующим образом.
Когда d-винную кислоту нагревают до 160°С в закрытом сосуде с небольшим количеством воды, сначала образуется винная кислота оптически недеятельная в поляризованном свете, затем рацемическая кислота, которая расщепляется в равных количествах на d-винную и Ζ-винную кислоты, тогда как недеятельная винная кислота расщепляться не может. Метавинную кислоту старой номенклатуры получают путем плавления d-винной кислоты. Если процесс остановить в момент перехода массы в расплавленное состояние, не превышая температуры 170— 180°С, винная кислота видоизменяется без потери массы. Если продолжать нагревание, винная кислота дает несколько ангидридов. В то время были описаны три производных винной кислоты: дивинная кислота (тартраловая или изовинная) С6Н10О11, растворимая тартреловая кислота и нерастворимый винный ангидрид С4Н4О5. Кальциевая соль дивинной кислоты растворима, тартреловая кислота может осаждаться ацетатом кальция. Наконец, при сухой перегонке винной кислоты наряду с другими продуктами образуются пировиноградная, уксусная и пировинная кислоты.
Чаттавей и Рей (1921) продолжили исследование разложения винной кислоты при нагревании. Проводя нагревание при пониженном давлении, они отметили в реакции две стадии. Сначала винная кислота теряет одну молекулу воды и образуется вещество (природы лактида) с потерей половины первоначальной кислотности. В действительности авторы ни разу не получили теоретически такого результата, и вещество, быстро растворившееся в воде, нейтрализуется щелочью, количество которой немного больше половины, необходимой для того, чтобы нейтрализовать исходную кислоту. Это вещество может быть снова превращено в винную кислоту путем гидролиза. Такая реакция может быть представлена в следующем виде:
СООН—СНОН—СНОН—СООН + СООН—СНОН—СНОН—СНОН
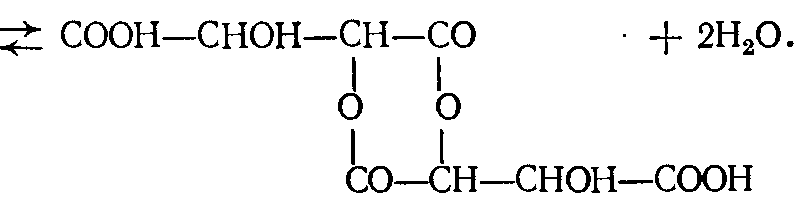
Во второй стадии потеря воды сопровождается различными процессами расщепления, в результате которых образуются окись углерода, углекислый газ, пировиноградная кислота и др.
Ни в одной из перечисленных работ не принимается во внимание необычное свойство продуктов, образующихся при нагревании винной кислоты, а именно способность ингибировать кристаллизацию солей винной кислоты. Порядок приготовления этих продуктов известен уже около полсотни лет, но эти интересные свойства их открыты лишь в последнее время. Первая опубликованная работа, посвященная продукту, ингибирующему кристаллизацию винного камня в винах, принадлежит Скаццола (1956).
В первой стадии нагревания молекулы винной кислоты подвергаются внутренней этерификации (образование сложного эфира), а затем происходит конденсация. Получаемый продукт более или менее полимеризован. Известно, что при нагревании из многих кислот-спиртов образуются гемиполилактиды. Эти вещества с открытой цепью включают две или несколько молекул кислоты-спирта, которые взаимно этерифицируются в сложные эфиры. Полимеризация происходит обязательно, поскольку она завершается очень интенсивной реакцией, в результате которой образуется нерастворимый продукт. Фактически продукт, полученный при разложении винной кислоты, тем менее растворим, чем продолжительнее нагревание. Растворы имеют тем более явные признаки коллоидов, чем продолжительнее нагревание.
Никогда не удается провести реакцию, в которой участвует 50% кислотных функций согласно формуле Чаттавея и Рея. Так как в большинстве случаев при этерификации связывается от 33 до 36% этих функций (максимум 39—40%), Скаццола (1956) отмечает, что это явление близко к тому, когда три молекулы винной кислоты, обладающие шестью кислотными функциями, теряют при этерификации две из них, т. е. 33%, и две молекулы воды. Схематически эту реакцию можно представить в следующем виде:
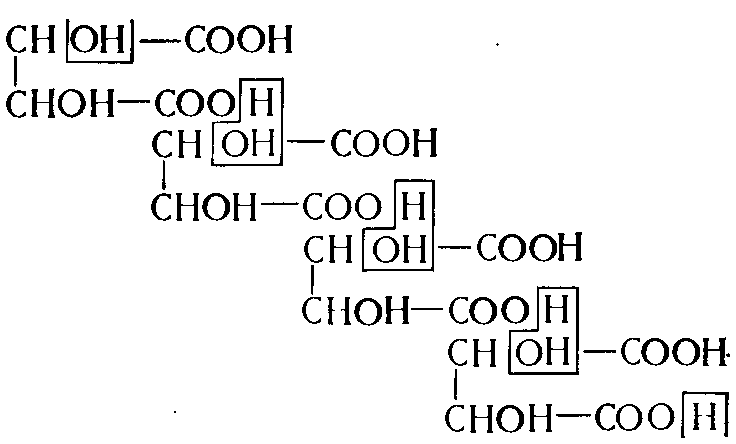
Относительно термина «метавинная кислота» следует сделать оговорку. Не нужно смешивать продукт, описанный под этим названием авторами прошлого столетия, который является изомером винной кислоты, получаемым путем простого плавления, с продуктом, который в настоящее время следует называть метавинной кислотой, который фактически получается в результате намного более глубокого разложения молекулы винной кислоты с потерей воды, перегруппировкой молекул и конденсацией и который соответствует определению внутренних сложных эфиров винной кислоты. Первый продукт совершенно лишен способности ингибировать кристаллизацию.
Таблица
Состав метавинной кислоты
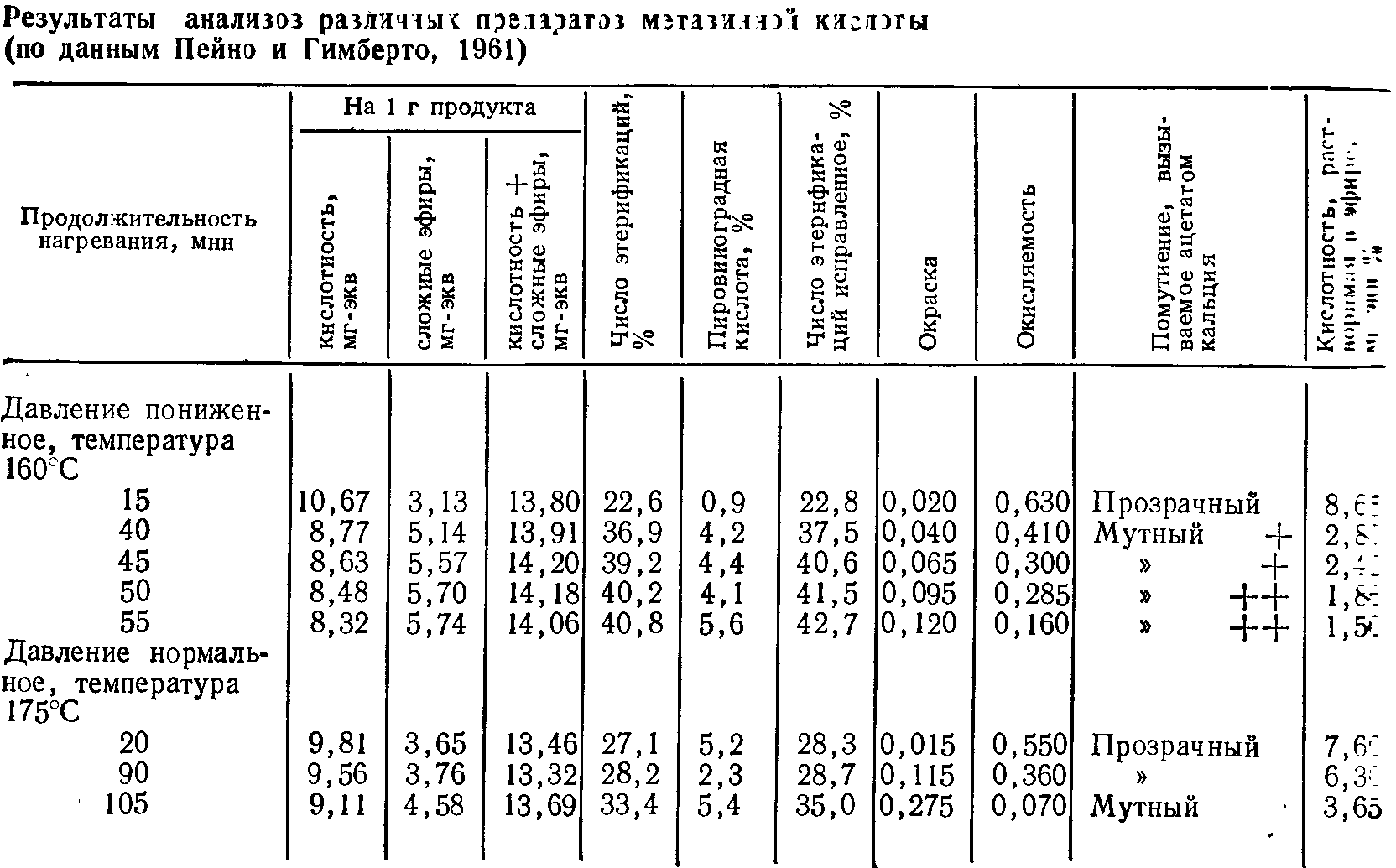
Согласно энологическому Кодексу, к основным компонентам этого продукта относятся сложный моноэфир и сложный диэфирдивинной кислоты в непостоянных количествах, получающиеся из двух молекул винной кислоты с потерей воды, смешанных с переменными количествами неэтерифицированной винной кислоты, пировиноградной кислоты и небольших количеств мало известных полиэфирных кислот. Пейно и Гимберто (1960, 1961) провели детальное исследование различных препаратов метавинной кислоты. Они определили показатель этерификации, растворимость в эфире, окисляемость перманганатом, осаждение ацетатом кальция, процентное содержание пировиноградной кислоты. В табл. 10.1 обобщены некоторые из этих результатов, полученных в строго определенных условиях. В результате фракционирования путем осаждения или экстрагирования и хроматографического анализа установлено, что каждый препарат метавинной кислоты следует рассматривать не как смесь определенных продуктов а как гомогенный (однородный) продукт, аналитические нормы которого всегда немного различны.
Показатель этерификации.
Определяют титруемую кислотность в присутствии фенолфталеина на 1 г продукта, который только что растворили. Поскольку кислотность 1 г винной кислоты равна 13,3 мг-экв, то в соответствии с данными предыдущего раздела кислотные функции винной кислоты исчезают во время нагревания.
Показатель этерификации препарата метавинной кислоты, энологическую ценность которого хотят установить, определяют методом омыления следующим образом: растворяют однородную пробу, состоящую из нескольких граммов метавинной кислоты, в небольшом объеме холодной воды. Если раствор содержит нерастворимые волокнистые обломки во взвешенном состоянии, его пропускают через бумажный фильтр, удаляя первую профильтрованную жидкость. Опытную пробу этого раствора нейтрализуют до изменения окраски фенолфталеина 0,1 н. раствором едкого натра. Количество опытной пробы подбирают так, чтобы шло от 10 до 15 см3 0,1 н. раствора едкого натра. Записывают использованный объем V. Затем к нейтрализованному раствору добавляют избыток 0,1 н. раствора едкого натра, равный объему V. Раствор оставляют в покое на 1 ч в закупоренном флаконе при температуре лаборатории, потом титруют остаточную щелочность 0,1 н. раствором серной кислоты. Пусть V' — объем добавленной жидкости. Проводят параллельно холостой опыт. Вычисляют индекс этерификации по формуле ![]()
Можно констатировать (см. табл. 10.1), что сумма кислотностей сложных эфиров тем больше показателя кислотности винной кислоты (13,3 мг- экв), чем продолжительнее и интенсивнее нагревание. Это следствие дегидратации. Потеря массы за счет потерь воды больше, чем потеря карбоксилов. Индексы этерификации очень изменяются в зависимости от продуктов, которые в этом случае исследуются. Они колеблются от 22 до 27% для кратковременного нагревания, до 40% — для более продолжительного нагревания. Препараты, полученные путем нагревания под вакуумом, обычно имеют самые высокие показатели. Индекс этерификации дает точный показатель эффективности продукта от виннокислых помутнений, поскольку ингибирующее действие его связано с содержанием сложных эфиров.
Пировиноградная кислота.
Пейно и Гимберто (1960, 1961) констатировали, что все образцы метавинной кислоты имеют реакцию на пировиноградную кислоту. Пировиноградная кислота образуется при нагревании расплавленной винной кислоты до точки кипения. При производстве метавинной кислоты под вакуумом можно собрать жидкость, которая представляет собой водный раствор пировиноградной кислоты концентрацией несколько граммов на 1 л. Таким образом, пировиноградную кислоту следует рассматривать как постоянную примесь в промышленной метавинной кислоте. Количественное определение проводят колориметрическим методом Дениже (1931), основанным на измерении интенсивности зеленого цвета, который появляется на холоде, когда к раствору пировиноградной кислоты добавляют уксусную кислоту, нитропруссид натрия и гидрат окиси аммония (нашатырный спирт). В пробирку помещают 1 см3 раствора метавинной кислоты концентрацией 40 г/л, затем последовательно добавляют 0,5 см3 уксуснокислого раствора концентрацией 40%, 3 см3 1%-ного раствора нитропруссида натрия и 1,5 см3 гидрата окиси аммония плотностью 22° Боме, разведенного наполовину. После каждого добавления производят перемешивание. Раствор оставляют в течение 1 ч и колориметрируют при 620 нм. Полученные значения сопоставляют с калибровочной кривой, построенной для двух растворов пировиноградной кислоты известной концентрации, и из этого делают вывод, в каком количестве она присутствует в анализируемом образце.
Пировиноградная кислота содержит около 1—6% по массе препаратов метавинной кислоты. Они обычно тем более насыщены, чем продолжительнее было нагревание. При работе в условиях пониженного давления ее образуется столько же, как и при нормальном давлении. В экстремальных условиях максимальное количество пировиноградной кислоты, добавляемой в вино, при 10 г/гл метавинной кислоты равно 5—6 мг/л — доза, которую можно не принимать во внимание. Присутствие пировиноградной кислоты немного искажает значение показателя этерификации. Если при вычислениях исключить влияние ее кислотности, получают несколько более высокие числа, как это видно из табл. 10.1.
Образование пировиноградной кислоты и ее конденсация, которая происходит при увеличении продолжительности нагревания, объясняют отчасти различия в окраске метавинных кислот и их запах, немного похожий на запах карамели. Этот запах сильнее в продуктах с более интенсивной окраской. Однако у хороших препаратов он никогда не бывает настолько сильным, чтобы ощущаться после добавления в вино. В табл. 10.1 окрашенность растворов выражена оптической плотностью, измеренной при 400 нм. Продукты, получаемые под вакуумом, окрашены намного слабее.
Окисляемость перманганатом на холоде объясняется содержанием примесей (соединений) пировиноградной кислоты. Как видно из табл. 10.1, окисляемость обратно пропорциональна значениям окраски раствора перманганата калия через две минуты после добавления одинакового количества различных метавинных кислот. В таких же условиях раствор винной кислоты этой же концентрации не восстанавливает перманганат и оптическая плотность составляет 0,799. Метавинные кислоты имеют тем большую восстанавливающую способность, т. е. содержат тем больше примесей, чем продолжительнее было нагревание, в результате которого их получили. Потеря воды при этерификации составляет около 10% для продукта с этерификационным числом 40, около 7,5% для продукта с числом 30. В действительности, потеря массы более значительна, так как образование пировиноградной кислоты сопровождается выделением углекислого газа и водяных паров. Общую потерю массы можно считать равной 20% для продукта с числом 40, полученного при нормальном давлении, и 10% для продукта с числом 30, полученного в таких же условиях.
Опыты по фракционированию метавинной кислоты.
Пейно и Гимберто (1960, 1961) пытались фракционировать раствор метавинной кислоты несколькими способами: путем дробной экстракции эфиром, фракционным осаждением в виде солей кальция. Хроматографическое разделение здесь не применимо, поскольку метавинная кислота легко гидролизуется в кислой или щелочной среде.
Растворимость различных препаратов метавинной кислоты в эфире колеблется от 1 до 4 (см. табл. 10.1). Она больше для продуктов, имеющих низкое этерификационное число. Растворимость в эфире изменяется в обратном порядке относительно этирификационного числа. Для этого измерения тщательно перемешивают 5 г метавинной кислоты в виде порошка со 100 см3 безводного эфира. Оставляют их в контакте на 24 ч с периодическим взбалтыванием смеси. Затем жидкость декантируют, фильтруют, удаляют путем испарения известный объем эфира и определяют остаток по массе (взвешиванием) или ацидиметрически. Эта операция сопровождается гидролизом некоторой части извлеченного продукта, ощутимым по снижению этирификационного числа. Это уменьшение могло бы навести на мысль, что сначала растворяются менее конденсированные формы и даже винная кислота в свободном состоянии. В действительности, коэффициент этерификации метавинной кислоты, как и остаток после экстрагирования, остается каждый раз практически постоянным. После трехкратной отмывки наблюдают уменьшение этирификационного числа всего на две единицы. С другой стороны, коэффициент растворимости препарата для каждого последующего извлечения представляет довольно постоянную величину. Метавинные кислоты ведут себя по отношению к экстракции эфиром как продукты гомогенные, не поддающиеся фракционированию.
Если 1 см3 насыщенного раствора ацетата кальция добавить к 10 см3 раствора метавинной кислоты концентрацией 40 г/л, то у некоторых препаратов наблюдают помутнение, обычно у тех, этерификационное число которых превышает 30%, тогда как другие остаются прозрачными. Зато когда прибавляют 5 см3 насыщенного раствора ацетата кальция к 10 см3 раствора метавинной кислоты концентрацией 100 г/л, возникает помутнение и, Как правило, наблюдается даже в случаях, когда продукт имеет низкое число. Поэтому было бы неточным утверждать, что только одна тартреловая кислота осаждается солями кальция, кроме метавинной и даже дивинной кислот. При обработке вин было бы также неправильно отказываться от тех препаратов, для которых эти соли вызывают помутнение. Осадок метатартрата кальция можно собрать при центрифугировании. Этот смолистый осадок плохо смешивается с дистиллированной водой, но растворяется в сильно разбавленной уксусной кислоте. Следовательно, можно было ожидать выделения таким путем наименее растворимой фракции с солью кальция, соответствующей наиболее активной части продукта. Однако опыт не подтвердил этой гипотезы. Таким путем нельзя разделить обогащенный и самый эффективный продукт и соли кальция имеющие то же эфирное число, как и у исходного препарата.
Следовательно, метавинную кислоту нельзя фракционировать. Каждый препарат представляет собой гомогенный продукт, определяемый эфирным числом, коэффициентом растворимости в эфире и кальциевой соли в воде. Возможен различный состав в зависимости от количества кислотных функций, участвующих в реакции. Максимум реакции кажется ограниченным и никогда не достигает 50%, предусматриваемых теорией, потому, что по мере того как развивается реакция, вероятность встречи между реакционными группами уменьшается и разложение начинается до завершения реакции.
Кроме того, в результате исследования физико-химических свойств метавинной кислоты получают мало данных о ее составе. Кривые титрования в кислой зоне могут накладываться на кривые винной кислоты, рК (3,45) соответствует среднему значению рК обеих винных функций.
Измерение ингибирующей способности кристаллизации
Как указывает Скаццола (1956), метавинная кислота представляет собой замечательный ингибитор кристаллизации винного камня и всех солей винной кислоты. Явление ингибирования можно показать следующим образом. В две пробирки, содержащие 10 см3 белого вина, добавляют 2 см3 раствора левовращающего тартрата аммония и 2 см3 уксусного раствора ацетата кальция (концентрацией 5%). В одну из двух пробирок вводят 2—3 капли раствора метавинной кислоты и все перемешивают. В контрольной пробирке практически мгновенно происходит осаждение рацемата кальция. В пробирке, получившей метавинную кислоту, оно задерживается на срок от нескольких часов до нескольких дней.
Таблица 10.
Содержание калия (в мг) в винах, обработанных различными дозами метавинной кислоты
№ продукта | Показатель этерификации | Количество метавинной кислоты, добавленное в каждую пробирку, мг | |||||
0,4 | 0,8 | 1,6 | 2,4 | 3,2 | 4,0 | ||
1 | 40,8 | 12,0 | 15,8 | 17,2 | 17,2 | 17,2 | 17,2 |
2 | 38,2 | 12,0 | 15,6 | 17,2 | 17,2 | 17,2 | 17,2 |
3 | 37,3 | 12,0 | 15,3 | 17,2 | 17,2 | 17,2 | 17,2 |
4 | 33,4 | 9,6 | 12,0 | 16,3 | 17,0 | 17,2 | 17,2 |
5 | 31,5 | 8,6 | 11,0 | 15,3 | 15,9 | 16,5 | 17,2 |
6 | 26,6 | 7,9 | 10,5 | 12,7 | 15,0 | 16,0 | 17,2 |
7 | 22,9 | 6,4 | 7,6 | 11,2 | 13,6 | 15,6 | 16,8 |
Примечание. Первоначальное содержание винной кислоты было 17,2 мг. Пробирка без метавинной кислоты сохраняет всего 5 мг калия.
Опыты по измерению растворяющей способности метавинной кислоты относительно виннокислых соединений можно проводить непосредственно с вином, например, по методике Шенара (1959). Она заключается в том, что в вино добавляют 4 г/л виннокислого калия или 2 г/л карбоната кальция и по истечении пяти дней выдерживания при низкой температуре в присутствии различных доз продукта отмечают появление кристаллического осадка.
Пейно и Гимберто (1960, 1961) разработали ускоренные методы проведения таких опытов, позволяющие оценивать путем сравнения практическую ценность препарата. Значение ингибирования изменяется соответственно химической природе кристаллов.
- В одну серию пробирок помещают 10 см3 насыщенного раствора битартрата калия (винного камня — кислого виннокислого калия КС4Н5О6). Добавляют различные дозы метавинной кислоты (от 0,4 до 4 мг) при одном и том же объеме (1 см3) и смешивают. Осаждение вызывается при добавлении 1 см3 96%-ного спирта и хранении пробирок в течение одной ночи при 0°С. В конце этого времени проводят фильтрование и определяют содержание остаточного калия в фильтрате с помощью пламенного фотометра.
В табл. 10.2 приведены результаты, полученные таким путем для семи промышленных образцов.
Продукты № 1, 2 и 3, число этерификации которых составляет от 37 до 40%, имеют практически одинаковую эффективность. Для получения таких же результатов требуется в два раза больше продукта с показателем этерификации 33%, в два с половиной раза при 31% и в три-четыре раза больше продукта с показателем от 23 до 26%.
- В другую серию пробирок помещают 10 см3 раствора винной кислоты концентрацией 3 г/л. Добавляют 2 см3 раствора метавинной кислоты в определенных количествах (от 0,7 до 4,2 мг). Все смешивают и добавляют 0,5 см3 насыщенного раствора ацетата кальция. Через 24 ч жидкость фильтруют и титруют оставшуюся в растворе винную кислоту в горячем состоянии 0,1 и. раствором перманганата калия. Вычитают количество перманганата, потребленного добавленной метавинной кислотой. В табл. 10.3 приведены результаты, полученные для тех же семи образцов.
Таблица 10.3
Содержание винной кислоты (в мг) в винах, обработанных различными дозами метавинной кислоты
№ продукта | Показатель этерификации | Количество метавинной кислоты, добавленное в каждую пробирку, мг | |||||
0,7 | 1 >4 | 2,1 | 2,8 | 3,5 | 4,2 | ||
1 | 40,8 | 31,6 | 31,6 | 31,6 | 31,6 | 31,6 | 31,6 |
2 | 38,2 | 31,6 | 31,6 | 31,6 | 31,6 | 31,6 | 31,6 |
3 | 37,3 | 30,6 | 31,6 | 31,6 | 31,6 | 31,6 | 31,6 |
4 | 33,4 | 28,9 | 29,9 | 30,3 | 31,6 | 31,6 | 31,6 |
5 | 31,5 | 21,8 | 29,4 | 29,6 | 29,8 | 31,6 | 31,6 |
6 | 26,6 | 18,5 | 28,3 | 28,7 | 29,1 | 29,1 | 31,6 |
7 | 22,9 | 12,5 | 19,5 | 24,3 | 29,6 | 30,0 | 30,0 |
Примечание. Первоначальное содержание винной кислоты было 31,6 мг. Пробирка без метавинной кислоты сохраняет только 6 мг винной кислоты.
При использовании лучших продуктов полное ингибирование кристаллизации тартрата кальция в лабораторных условиях получают при меньших дозах, чем в случае с битартратом калия (винным камнем). Когда применяют продукты с более низким показателем этерификации, при равных дозах получается почти одинаковое действие при обоих типах осаждения. Ингибирование осаждения кальция в большей степени зависит от качества метавинной кислоты, чем при образовании осадка калия. Чтобы ингибирование было полным, в данном случае нужно было иметь несколько больше продукта с показателем этерификации 37, чем с показателем 40. Потребовалось использовать приблизительно в четыре раза больше препарата с показателем этерификации 33, в пять раз больше с показателем 31, в шесть раз больше с показателем 26 и еще больше с показателем 23. На практике защита продуктом № 1 в дозе 2 г/гл оказывается столь же эффективной и может быть даже лучше, чем продуктом № 6 в дозе 10 г/гл.
- Предыдущие опыты требуют затраты целого рабочего дня для получения результатов. Если же работу проводить на основе осаждения рацемата кальция, более быстрого, чем осаждение солей винной кислоты, можно получить данные об ингибирующей способности через 1 ч.
В серию пробирок вводят 10 см3 d- винной кислоты концентрацией 3 г/л. Затем добавляют в одинаковом объеме (1 см3) некоторое количество метавинной кислоты, изменяющееся от 0,5 до 15 мг. Все перемешивают и добавляют 0,5 см3 раствора /-тартрата аммония (2%) и 0,5 см3 уксусного раствора ацетата кальция. Наблюдают за появлением осадка рацемата кальция и отмечают для каждой партии метавинной кислоты минимальное количество, необходимое для предотвращения осаждения в течение 1 ч. При исследовании промышленных продуктов, перечисленных выше, были получены следующие дозы-пороги:
![]()
Различия в активности в зависимости от препаратов здесь намного более значительны, чем в других опытах, к тому же этот опыт выполняется быстрее и он более чувствителен. Он подтверждает предыдущие наблюдения и показывает, что ингибирующая способность хорошо выражается показателем (числом) этерификации.
Промышленные продукты, содержащие метавинную кислоту, по качеству разделяют на три вида: продукты с показателем этерификации от 36 до 40, обладающие наибольшей эффективностью; продукты с показателем 30—35, качество которых считается средним и, наконец, продукты с показателем менее 30, не обладающие достаточной эффективностью и плохо подходящие для обработки вин. Энологический кодекс установил как минимальное содержание этерифицированной кислоты 32 %.
Согласно этому же кодексу эффективность метавинной кислоты определяют следующим образом. Приготовляют раствор концентрацией 2 г/л в холодной воде. Для этого в флакон вместимостью 20 см3 помещают 20 см3 насыщенного водного раствора битартрата калия; 0,5 см3 раствора метавинной кислоты концентрацией 2 г/л и 2,0 см3 95%-ного спирта.
Жидкость тщательно перемешивают взбалтыванием и ставят в холодильник с температурой 0°С на 12 ч. Из каждого прозрачного раствора отбирают по 11,25 см3 и титруют кислоту 0,1 и. раствором гидроксида натрия в присутствии фенолфталеина. Обозначим число кубических сантиметров см3, использованных в присутствии метавинной кислоты, через п, через п' тоже число в ее отсутствии и через п" то же, но в случае насыщенного раствора битартрата калия. Тогда п должно быть, по меньшей мере, равно 0,8 п", тогда как п' должен быть около одной трети п".
Механизм ингибирования
Обычно считают, что метавинная кислота покрывает оболочкой субмироскопические зародыши винного камня и, таким образом, препятствует их росту. Когда наблюдают под микроскопом кристаллы, образовавшиеся, несмотря на присутствие метавинной кислоты, вследствие того, что использованная доза была очень малой, констатируют нарушение процесса и аномалии кристаллизации. Действие продуктов, препятствующих осаждению и образованию осадка карбоната кальция в воде, объясняли адсорбцией на поверхности частиц в процессе кристаллизации.
Прежде всего необходимо напомнить об общем процессе образования кристаллов, который применим и к появлению кристаллов виннокислых солей в вине. Кристаллы могут образовываться из перенасыщенных растворов. Их появление обусловливают два явления: возникновение кристаллических зародышей (начальных точек кристаллизации), рост или развитие кристаллов. Образование кристаллов может происходить только в присутствии зародышей. Трудность возникновения зародышей, которой зачастую объясняется возможность очень длительного состояния перенасыщения, связана с тем, что она требует создания новой поверхности разделения. Зародыши сами по себе могут образовываться только тогда, когда в жидкости присутствуют твердые тела, представляющие некоторую аналогию со структурой атома. В этих процессах большую роль обычно играют перегородки. Когда они по своей кристаллографии аналогичны (емкости с отложениями винного камня на стенках и дне), процесс кристаллизации протекает легче.
В ином случае аналогия с размещением элементов атома может все же существовать в деформированных местах. Так, природа поверхности стекла, его чистота, наличие шероховатостей оказывают влияние на образование осадка в бутылках.
С момента появления зародышей кристаллы развиваются, «питаются» за счет постепенно возрастающего слипания молекул в соответствии с геометрической архитектурой различных систем, которая обусловливает их общую форму. Новые составные части сначала адсорбируются на поверхности кристалла, прежде чем занять место в структуре решетки.
Ингибирование кристаллизации метавинной кислотой проявляется в том, что она с самого начала препятствует росту кристаллов, останавливая накопление из-за тех же поверхностных явлений. Так, некоторые адсорбируемые вещества могут видоизменить процесс развития кристаллов и их форму. Адсорбция бывает более интенсивной у тех веществ, которые имеют относительно большее сродство с твердым телом, чем с растворителем.
В интересующем нас случае происходит адсорбция метавинной кислоты в коллоидном состоянии на поверхность кристаллического зародыша, приостанавливающая его рост именно в тех точках, где происходит адсорбция макромолекул метавинной кислоты. Крупные молекулы метавинной кислоты, которые не кристаллизуются, включаются в решетку виннокислого криссталла и покрывают его, блокируя, таким образом, процесс «питания», т. е. увеличение размеров кристалла. Когда ингибирование бывает лишь частичным, кристаллы продолжают образовываться в той же кристаллической системе, но принимают неправильные (ненормальные) формы. На рис. 10.1 и 10.2 представлены микрофотографии (с увеличением в 75 раз) кристаллов кислого виннокислого калия и виннокислого кальция (нормальных и деформированных метавинной кислотой). Деформация происходит в результате неодинакового роста кристалла в различных плоскостях.
Кантарелли (1963) констатировал, что эффект ингибирования зависит не только от действия метавинной кислоты. Этот автор получил полимеризованные лактиды из других оксикислот, найденных в винах, таких, как яблочная, лимонная и молочная. Он смог проверить, что все эти продукты обладают способностью тормозить кристаллизацию. Это относится и к гуммиарабику, пектину, карбоксиметил- целлюлозе.
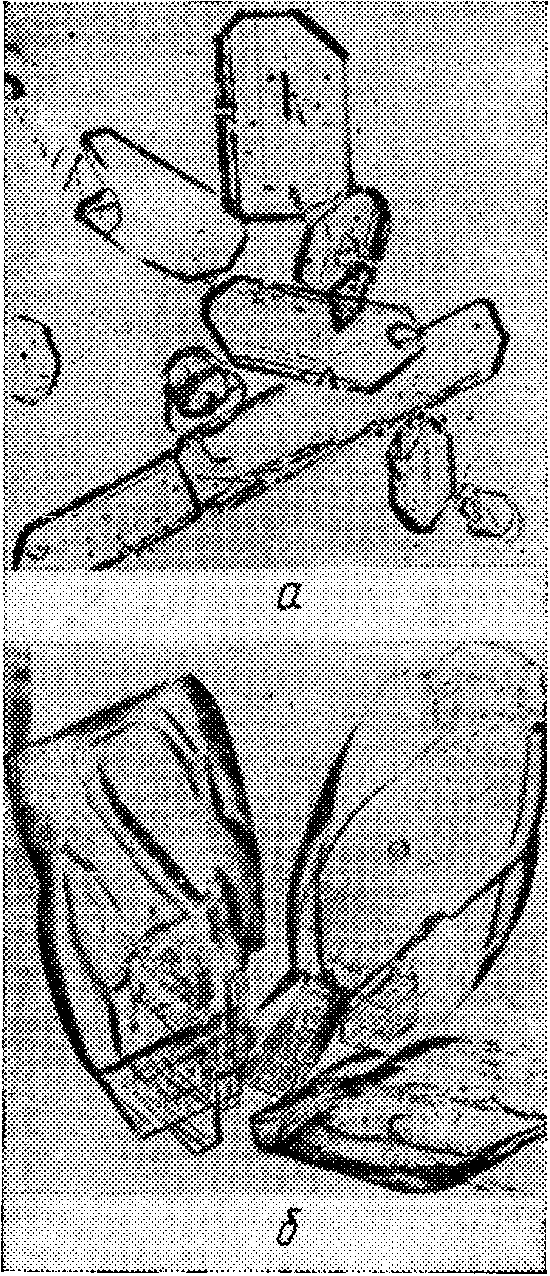
Рис. 10.1. Кристаллы битартрата калия (Х75), образовавшиеся:
а — в нормальных условиях; б — в присутствии метавинной кислоты.

Рис. 10.2. Кристаллы тартрата кальция (Х75), образовавшиеся:
а — в нормальных условиях; б — в присутствии метавннной кислоты.
Нестабильность метавинной кислоты
В разделе, где было описано определение способности к ингибированию, приведены примеры, которые показывают большую эффективность метавинной кислоты для блокирования нерастворимости битартрата калия и виннокислого кальция. Этот же самый эффект обнаруживается и в применении к вину. При введении метавинной кислоты в молодые вина в дозе 100 мг/л любое кристаллическое осаждение прекращается на несколько месяцев. Вина, хранящиеся на холоде, не дают никакого осадка и при очень низких температурах, и можно даже замораживать вино, которое после оттаивания также не дает никаких виннокислых помутнений и осадков. Но в водном растворе метавинная кислота нестабильна, она склонна к медленному гидролизу. Именно скоростью гидролиза обусловлена продолжительность периода, в течение которого она бывает эффективной.
В твердом состоянии при хранении в герметически закрытой емкости, исключающей доступ влажного воздуха, этот продукт может сохранять свою активность неограниченно долгое время. Но он очень гигроскопичен, и при контакте с влажным воздухом его поверхность размягчается и разжижается с одновременной потерей эффективности.
В растворе наблюдается непрерывное уменьшение показателя этерификации, и метавинная кислота в результате гидратации и гидролиза проявляет тенденцию возвратиться в состояние винной кислоты. На рис. 10.3 показан ход этого процесса в 2%-ных растворах (pH 2,0), хранившихся при температуре лаборатории (18—20°С), для двух видов метавинной кислоты.
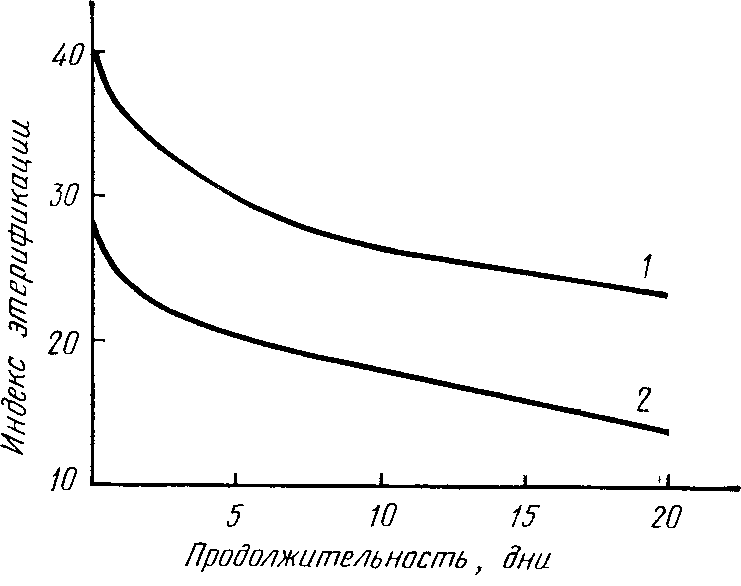
Рис. 10.3. Скорость гидролиза 2%-кого раствора метавинной кислоты (t=18—20°С), сопровождающегося уменьшением индекса этерификации: 1 — метавинная кислота № I; 2— метавинная кислота № 2.
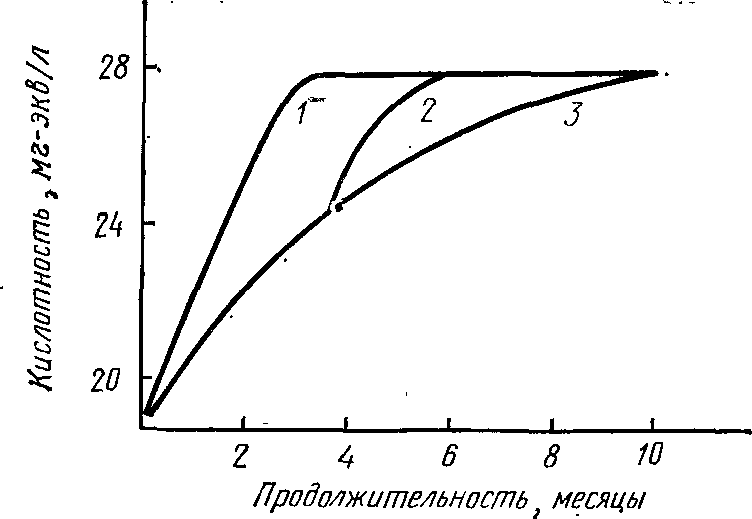
Рис. 10.4. Скорость гидролиза раствора метавинной кислоты концентрацией 2 г/л, сопровождающегося повышением титруемой кислотности при температуре (в °C) (по данным Карафа, 1958): 1 — 23; 2 — сначала 5, затем 23; 3 — 5.
После быстрого снижения в первый день гидролиз продолжается с уменьшением показателя в среднем на 1 % в день. Карафа (1958) проследил даже гидролиз раствора метавинной кислоты концентрацией 2 г/л в зависимости от температуры. Раствор хранят при температуре окружающей среды (20—23°С) и в холодильнике (при 4—5°С). На рис. 10.4 показано, что гидролиз завершился через 3 мес. при обычной температуре и через 10 мес. при низкой температуре.
Такое же явление гидролиза наблюдается в вине после введения в него метавинной кислоты. Основными факторами являются pH и температура. Кантарелли (1961) рекомендует применять для вин с повышенной кислотностью более высокие дозы. Карафа (1958) проследил потерю эффективности в вине, обработанном метавинной кислотой концентрацией 10 г/гл и хранившемся при двух различных температурах. Через месяц в необработанном вине появился обильный кристаллический осадок. При хранении в условиях температуры 20—23°С осадок появился через 3 мес. после добавления метавинной кислоты, тогда как при 4— 5°С он образовался только на десятый месяц.
На основе собственного опыта, полученного с большим числом образцов различных вин, авторы пришли к следующим выводам: при постоянной температуре, близкой к 0°С или даже ниже (при хранении вин в холодильнике), продолжительность ингибирующего действия достигает нескольких лет: при 10—12°С (заводы шампанских вин) она превышает два года; при температурах от 10 до 16°С, свойственных подвалам для хранения вин после розлива в бутылки, продолжительность ингибирования может быть около 18 мес. При температуре от 12 до 18°С некоторые вина начинают давать осадок через год. В термостате, отрегулированном на 20°С, ингибирование прекращается через 3 мес. и при 25°С через один месяц. В то же время гидролиз метавинной кислоты при 30°С завершается за неделю, а при 35—40°С за несколько часов. Эти и аналогичные наблюдения, на первый взгляд, кажутся парадоксальными и объясняются гидролизом при несколько повышенной температуре: обработанное таким образом вино дает осадок тартрата кальция при хранении в условиях температуры от 20 до 25°С, тогда как за это же время при хранении в холодильнике осаждения не происходит.

