Разложение гексоз гетероферментативными бактериями — молочнокислое скисание
Гетероферментативное брожение, вызываемое молочнокислыми бактериями, открыли в 1894 г. Гайон и Дюбург в испорченных винах, содержащих большое количество маннита, что и дало основание называть эту болезнь маннитным брожением. Авторы показали, с одной стороны, образование большого числа продуктов брожения, с другой — различное поведение глюкозы и фруктозы, причем последняя является специфической для образования маннита. В противоположность гомоферментативному брожению молочная кислота является не единственным продуктом, она даже количественно не самая большая (см. табл. 15.4). Понятно, что балансы такого (брожения сильно изменяются в зависимости от видов бактерий и условий их развития.
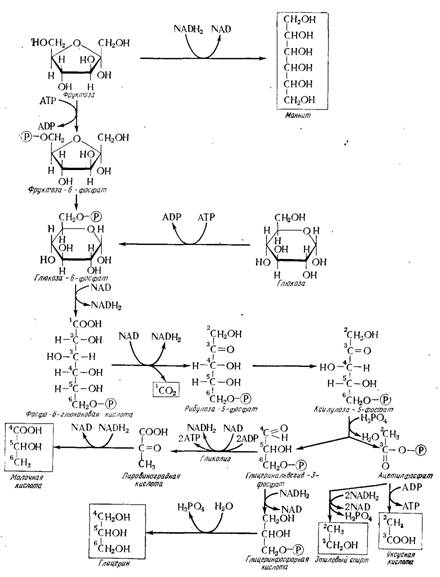
Рис. 15.26. Схемы гетеромолочнокислого сбраживания глюкозы и фруктозы. Образующиеся при этом продукты заключены в прямоугольники.
Действующие здесь механизмы отличаются от тех, какие характеризуют гомоферментативное брожение: первые реакции относятся к циклу пентоз и идут по (классическому пути разложения углеводов гликолизом (рис. 15,26). Глюкоза-6 фосфат, получающаяся как из -глюкозы, так и из фруктозы, является исходным пунктом разрыва молекулы сахара. Этот сложный эфир окисляется в фосфо-6- глюконовую кислоту, которая сама подвергается окислительному декарбоксилированию, ведущему к пентое-рибозе-5 фосфату. Изомеризация пентоз ведет к ксилозе-5-фосфату, разрыв молекулы которой дает ацетил- фосфат (С2) и тлицеринальдегид-З- фосфат (Сз). Последний вновь подвергается гликолизу, образовавшаяся же пировиноградная кислота восстанавливается в молочную кислоту. Другой механизм обеспечивает переход глицеринальдегида-3-фосфата в глицерин, поскольку восстановление возможно благодаря NADH2, получающемуся от гликолиза; в этом случае происходит истинное глицерино-пировиноградное брожение и одна часть пировиноградной ,кислоты, которая не может быть восстановлена в молочную кислоту, служит для образования вторичных продуктов (уксусной кислоты, янтарной и бутандиола-2,3), показанных в табл. 15.4, по общим механизмам (см. рис. 15.11).
Со своей стороны ацетилфосфат восстанавливается в этиловый спирт. Это восстановление необходимо для обеспечения вторичного окисления NADH2 в форму NAD. Действительно, если не учитывать образование глицерина, которое наблюдается во время этого процесса, 3 молекулы NAD восстанавливаются, причем две для окисления глюкозы и одна для окисления глицеринальдегид-З-фосфата. Один из них повторно окисляется за счет пировиноградной кислоты, два других за счет ацетилфосфата. Таким образом, баланс гетероферментативного брожения в этой форме может быть записан (без учета возможного глицерино-пировиноградного брожения) следующим образом:
С6Н1206^ СН3 - СНОН - СООН +
Глюкоза Молочная кислота
+ СН3 - СН2ОН + С02. (1.)
Этанол
Но бактериальная клетка может располагать экзогенным акцептором водорода (или, что то же самое, электронов), т. е. веществом, присутствующим в питательной среде и способным проникать внутрь клетки, где оно подвергается восстановлению (Барр, 1972). В этом случае акцептор обеспечивает вторичное окисление двух молекул 2NADH2 вместо ацетилфосфата, который тогда сможет быть гидролизованным в уксусную кислоту с освобождением одного АТФ и, следовательно, дополнительной энергии. Трудность восстановления органических кислот (уксусная) отражает предпочтительное восстановление экзогенного акцептора. Обозначая акцептор через А, можно выразить баланс гетероферментативного брожения в следующем виде:
С6Н1206 + 2А СН3 - СНОН - СООН +
Глюкоза Молочная кислота
+ СН3 - СООН + С02 + 2АН2. (2>
Уксусная кислота
При натуральном брожении уравнения (1) и (2), равно как и при глицерино-пировиноградном брожении, могут функционировать одновременно. В случае сбраживания фруктозы этот сахар может сам служить акцептором водорода А и именно поэтому источником маннита; этот же механизм объясняет образование небольших количеств других многоатомных спиртов: эритрита с С4 и арабита с С5 (Гимберто, 1969; Дюберне и сотрудники, 1974). Соответствующие сахара являются промежуточными звеньями цикла пентоз, реакции которого обеспечивают в схеме гетероферментативного брожения переход глюкозы-6-фосфата в ксилозу-6-фосфат. Опираясь на эту теорию и данные табл. 15.4, отмечают, что в гетероферментативном сбраживании фруктозы не происходит восстановления ацетилфосфата и, следовательно, образования этанола, который появляется исключительно при сбраживании глюкозы.
Схема этой совокупности механизмов (см. рис. 15.26) показывает, что чистое гетероферментативное брожение [см. уравнение (1)] обеспечивает освобождение одной молекулы АТФ во время разложения молекулы глюкозы. В уравнении (2) выигрыш энергии больше и соответствует двум молекулам АТФ.
Новый тип гетероферментативного брожения выявили Барр и сотрудники (1971) у некоторых Betabacterium, выделенных из вина; он характеризуется отсутствуем экзогенного акцептора водорода.
Пейно и сотрудники (1967) показали, что гетероферментативные койки, выделенные из вина, образуют исключительно -молочную кислоту D(—); некоторые гетероферментативные бациллы обладают такой же характеристикой, хотя большинство их образуют одновременно молочную кислоту D(—) и молочную кислоту L(+) с преобладанием второй. Известно, что процессы развития бактерий в винах ведут к образованию различных летучих кислот (муравьиная, пропионовая, масляная) в концентрациях порядка нескольких граммов на литр). Механизмы их образования из пировиноградной кислоты показаны на рис. 15.11.
Разложение пентоз
Виноградный сок содержит две пентозы — арабинозу и ксилозу. Некоторые винные бактерии используют оба сахара, другие — один из них, наконец, существуют такие, которые не воздействуют на пентозы. Действие на пентозы не связано с гомо- или гетероферментативным характером брожения, который относится исключительно к сбраживанию глюкозы. Разложение пентоз происходит всегда с образованием уксусной кислоты; она может быть источником небольшого повышения летучей кислотности красных вин, выдерживаемых в деревянных бочках. Деградация молекул пентозы осуществляется посредством ксилозы-5-фосфата, механизмы разложения которого описаны в разделе, относящемся к гетероферментативному брожению гексоз (см. рис. 15.26).
Рис. 15.27. Различные механизмы ферментативного разложения яблочной кислоты. (MDH- маликодегидрогеназа; яблочный фермент; ffML-яблочно-молочный фермент; LDH-лактико- дегидрогеназа).
В личном сообщении д-р Лондон (Национальный институт здравоохранения, Мериленд, США) подтверждает существование двух ферментов, способных использовать яблочную кислоту (независимо от маликодегидрогеназ). Наиболее известный в биохимии истинный яблочнокислый фермент проявляет максимальную активность при рН 8,5 и не синтезируется клетками, культивируемыми в среде, богатой глюкозой. Как было показано выше, он превращает яблочную кислоту в пировиноградную (см. рис. 15.27), а образование молочной кислоты связано с возможным присутствием лактикодегидрогеназ; в этом случае оптическая природа образующейся молочной кислоты зависит от природы присутствующих лактикогидрогеназ.
Другой, менее известный фермент, который наиболее правильно было бы называть «яблочно-молочным ферментом», имеет максимум активности в кислой среде, и его синтез не подавляется присутствием большого количества глюкозы; его часто смешивают с яблочным ферментом в собственном смысле слова. Именно этот фермент участвует в яблочно-молочном брожении (Лонво, 1975), он превращает яблочную кислоту непосредственно в молочную, но возможные промежуточные реакции пока что не известны (см. рис. 15.27, реакция III). Возможно, что речь идет о простом декарбоксилировании, хотя этот тип реакции у гидроксилированной кислоты редко встречается в биохимии. Можно также предполагать, что промежуточным звеном является пировиноградная кислота и она остается фиксированной на белковой поверхности фермента, где восстанавливается в молочную кислоту самим яблочно-молочным ферментом, который в таком случае должен был бы обладать двумя видами активности. Таким образом, можно было бы объяснить невмешательство лактикодегидрогеназ и стереоспецифичность реакции и, следовательно, образование исключительно лишь молочной кислоты L(+). Лонво и Риберо- Гайон (1973) показали значение углекислотного электрода для исследования механизма этой реакции.
Более точно свойство яблочного фермента молочнокислых бактерий, выделенных из вина, определил Лафон-Лафуркад (1970). Этот автор показал, что в подавляющем большинстве штаммы обладают ферментом, активность которого не зависит от условий предшествующей культуры, некоторые же обладают индуктируемым ферментом, т. е. синтез которого индуктируется, если в питательной среде содержится яблочная кислота. Наконец, другие штаммы не проявляют никакой ферментативной активности, каковы бы ни были условия предшествующей культуры. Этот признак имеет важное значение для отбора штаммов, пригодных для использования в виноделии.
Известно, что реакция преобразования яблочной кислоты в молочную не сопровождается выделением энергии, которая могла бы использоваться химическим путем, это реакция эндогенного типа. Следовательно, это явление не является настоящим брожением, оно не позволяет бактериальным клеткам находить энергию, необходимую для их роста и размножения. Таким образом, яблочно-молочное брожение можно объяснить, только допуская возможность развития бактерий за счет других элементов вина, например, углеводов или азотистых веществ. Радлер (1958) подтвердил, что сахара должны неизбежно служить источником энергии для бактерий яблочно-молочного брожения, но необходимые количества исключительно малы; 1 г яблочной кислоты разлагается 10 мг бактерий (в сухой массе), которые требуют для своего роста 0,1 г сахара. В гетероферментативном брожении такое же количество сахара дает только 50 мг молочной кислоты, 26 мг спирта и 22 мг углекислого газа.
Азотистые вещества также могли бы служить источником энергии. В действительности, паралле.чыю с яблочно- молочным брожением наблюдается снижение белкового азота вина, следующее за увеличением содержания аммиачного азота вследствие дезаминирования органических азотистых веществ.
Наконец, не исключено, что другие компоненты вина могут служить источником энергии для развития бактерий яблочно-молочного брожения. В частности, мезоинозит, средняя концентрация которого составляет 0,5 г/л, иногда исчезает в ходе этого явления, и его концентрация может даже упасть до нуля (Пейно и Лафон-Лафуркад, 1955). Такое разложение мезоинозита происходит без образования летучих кислот.
Разложение лимонной кислоты
О деградации лимонной кислоты молочнокислыми бактериями с образованием летучей кислотности известно с давних пор. В частности, известно, что яблочно-молочное брожение иногда сопровождается более или менее глубоким разложением лимонной кислоты, которая ответственна за увеличение летучей кислотности, наблюдаемое во время брожения.
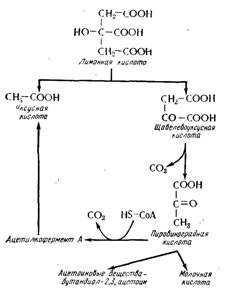
Рис. 15.28. Разложение лимонной кислоты молочнокислыми бактериями.
Исследуя баланс этого разложения, Шарпантье и сотрудники (1951) и Шарпантье (1954) показали, что одна молекула лимонной кислоты дает от 1,2 до 1,5 молекулы уксусной кислоты, очень малое количество молочной кислоты и от 0,2 до 0,3 молекулы ацетоиновых веществ (бутандиол-2,3 и ацетоин). Основываясь на предыдущих работах и на результатах собственных исследований, эти авторы предложили механизм деградации, включающий разрыв лимонной кислоты на щавелево-уксусную кислоту и уксусную (рис. 15.28). Первая декарбоксилируется в пировиноградную кислоту, которая сама по себе лежит в основе молочной кислоты, с одной стороны, и ацетоиновых веществ (бутандиол-2,3 и ацетоин), с другой, посредством описанных выше реакций (см. рис. 15.11). Эта пировиноградная кислота может также образовывать уксусную кислоту с помощью ацетилко- фермента А с образованием одной молекулы СО2 или в некоторых случаях муравьиной кислоты (см. рис. 15.11). Эта схема, которая включает двоякий источник уксусной кислоты, построена с учетом образования более одной молекулы этой кислоты на одну молекулу разложенной лимонной кислоты.
Разложение глицерина — болезнь прогоркания
Использование глицерина бактериями и особые характеристики, которые оно придает вину, описано многими авторами, хотя этот случай встречается относительно редко. Однако механизмы, посредством которых осуществляется это разложение, остаются невыясненными. Кроме того, не определен баланс этого превращения, аналогичный приведенному выше относительно разложения лимонной кислоты. Рис. 15.(29 составлен на основе общих сведений о разложении глицерина различными микроорганизмами. С одной стороны, это вещество превращается в пировиноградную кислоту сначала путем реакций, обратных реакциям глицерино-пировиноградного брожения (см. рис. 15.14), и затем путем гликолиза (см. рис. 15.10), с другой — оно трансформируется в акролеин и пропандиол-2,3 посредством особого механизма.
Таким образом, наряду с классическими продуктами бактериального метаболизма отмечают образование акролеина, который -является ответственным за особые органолептические характеристики «прогорклых вин» вследствие его связи с фенольными соединениями (Ренчлер и Таннер, 1951). Сбраживание глицерина дает также пропандиол-3 (Вуд, 1961), присутствие которого в больных винах кажется пока недоказанным. Наконец, обнаруживается муравьиная кислота (Вуд, 1961), которая получается от перехода пировиноградной кислоты в уксусную с помощью ацетилкофермента А (см. рис. 15.11).
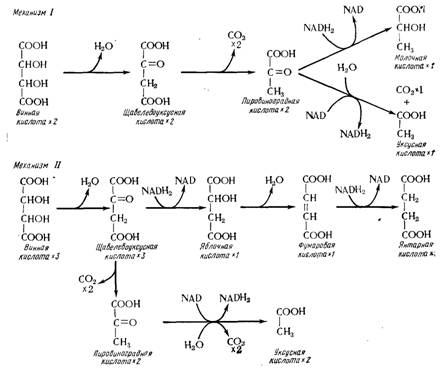
Рис. 15.30. Разложение винной кислоты молочнокислыми бактериями (Радлер и Янисис, 1972).

Рис. 15.29. Разложение глицерина молочнокислыми бактериями.
Разложение винной кислоты — пропионовокислое брожение (турн)
Лишь ограниченное ч-исло молочнокислых бактерий вина способно разлагать винную кислоту. Это разложение представляет собой серьезную болезнь вина — турн, иногда довольно частое явление, но в настоящее время встречающееся все реже и реже вследствие прогресса в технике хранения вина.
Механизм разложения винной кислоты исследовали Крампиц и Линен (1964) и особенно Радлер и Янисис (1972).
Из анализа балансов, полученных на различных штаммах, Радлер и Янисис сделали вывод, что известны два пути разложения винной кислоты (рис. 15.30). Lactobacillus plantarum используют механизм I, который соответствует образованию из двух молекул винной кислоты трех молекул С02, одной молекулы уксусной кислоты и одной -молекулы молочной кислоты. Lactobacillus brevis использует механизм II, который соответствует образованию из трех молекул винной кислоты четырех молекул С02, двух молекул уксусной кислоты и одной молекулы янтарной кислоты. В этих двух механизмах обеспечивается равновесие окисления-восстановления в том смысле, что число молекул NAD, восстанавливаемых в NADH2, равно числу молекул NADH2, окисляемых в NAD.
Рис. 15.32. Продукты окисления сахаров уксуснокислыми бактериями.

Рис. 15.31. Окисление спирта в уксусную кислоту за счет кислорода воздуха уксуснокислыми бактериями.
Некоторые бактерии могут реализовать частичное окисление уксусной кислоты в С02 и Н20, и соответствующая характеристика служит тестом для их классификации (Дивие и Дюпюи, 1969). Уравнение записывается: СН3 — СООН + -202 2С02 + 2Н20.
В этом случае общее уравнение уксуснокислого брожения приобретает вид
СН3 — СН2ОН + 302 2С02 + ЗН20.
Точно так же уксуснокислые бактерии вызывают частичную этерификацию уксусной кислоты этиловым спиртом в соответствии с реакцией
СН3 - СООН + сн3 — сн2он
сн3 — со — о — сн2 — СНз + н2о,
Этилацетат играет важную роль в энологии; он ответственен за особые органолептические качества вин, пораженных при уксусном скисании.
Окисление сахаров
Кетогенность уксуснокислых бактерий обычно используется как тест классификации. Она соответствует их способности окислять сахара с образованием веществ, обладающих функцией кетонов. Различие между сахарами и этими кетоновыми (веществами показано на рис. 15.32, который не предусматривает тесноовязанных механизмов и промежуточных реакций. О многих из этих веществ сообщали Вюрдиг и Шлоттер (1969), а также Салис а Пейно (1971). Кетоновые вещества присутствуют во всех винах, но их особенно много в винах, полученных из винограда, на котором гниль вызвала растрескивание ягод и развитие уксуснокислых бактерий. Кетоновые вещества также участвуют в связывании сернистого ангидрида.
* Заполнение бочки бродящим суслом под шпунт может привести к вспениванию сусла и вытеканию пены через шпунтовое отверстие, что приведет к потерям сусла и нарушению санитарного состояния бродильного отделения (прим. спец. ред.).

