Признаки медного касса
В белых винах, содержащих свободную сернистую кислоту и выдерживаемых без доступа воздуха в бутылках, иногда появляется помутнение, которое постепенно дает красно-бурый осадок. Если бутылки находятся в лежачем положении, осадок приобретает вид лепешки на плечике и коричневатой полосы на нижней стенке корпуса бутылки. В винах, содержащих белки, появляются бурые хлопья. Если помутневшее вино имеет контакт с воздухом или насыщается кислородом при перемешивании на воздухе, муть и осадок исчезают через несколько часов или несколько дней; если осадок хлопьевидный, он обесцвечивается. В осадке всегда содержится большое количество меди. Карль первым описал этот порок вина и указал на присутствие меди. Мутность появлялась только в винах, содержащих значительную дозу этого металла, например более 0,5 мг/л. Достаточно добавить 1 мг/л вина в виде сульфата к белому сульфитированному вину, не имеющему контакта с воздухом, чтобы появилась муть. Это основное доказательство той важной роли меди, которую она играет в данном процессе. Наконец, удаление меди (желтой кровяной солью) противодействует появлению мути в винах, склонных к помутнению. Такое помутнение принято называть «медным кассом», при этом медь осадка находится в двухвалентном состоянии.
Образование мути очень ускоряется небольшим повышением температуры вина, и на практике оно происходит главным образом летом. В это время помутнение может образовываться не только в бутылках, но также и в чане или в герметически закрытой бочке. Медный касс особенно ускоряется на свету. Если вина в бутылках из белого стекла выдержать на солнце, то очень быстро появляется муть (через несколько часов) при условии достаточно высокой концентрации меди.
Иногда можно наблюдать, что бутылки, остававшиеся прозрачными в течение многих месяцев или даже лет при хранении в темноте, уже через несколько дней мутнеют, когда их просто переносят на другое место.
Отмечают, что до начала помутнения еще прозрачное вино становится несколько более окрашенным по сравнению с контрольными образцами, не содержащими меди, и в дальнейшем появляется мутность и красно-коричневый осадок. Это наблюдение показывает, что здесь также следует различать химические процессы, ведущие к образованию нерастворимого вещества, но прежде всего в прозрачном коллоидном растворе, и физико-химические, выражающиеся в флокуляции этого коллоида. Иногда, особенно в винах, лишенных белков, флокуляция коллоида, ответственного за порок вина, может быть вызвана простым взбалтыванием или перемешиванием.
Содержание меди в белых винах можно определить довольно простыми способами. Колориметрический анализ довольно точен, но на практике можно производить следующее качественное испытание (тест). 20 см3 вина, подлежащие исследованию, помещают в две пробирки; в одну вводят несколько капель свежего раствора 1%-ного моносульфида натрия. Жидкость тщательно перемешивают и наблюдают на белом освещенном фоне в продольном направлении оттенки окраски в обеих пробирках. Если вино не содержит меди или только несколько десятых миллиграмма на 1 л, обе пробирки имеют одинаковый оттенок. Если же меди содержится больше, пробирка, в которую внесен сульфид, приобретает более интенсивную, более коричневую окраску. При небольшом навыке, оперируя на винах, содержащих известные дозы, можно приближенно определять, содержит ли данное вино 0,5; 1 или 2 мг/л меди.
Механизм образования медного касса
Один из авторов этой книги обнаружил присутствие сероводорода в осадке медного касса наряду с медью. В этом нетрудно убедиться, нагревая вместе с соляной кислотой достаточное количество центрифугированного и промытого осадка; бумага, пропитанная основным нитратом свинца и помещенная у отверстия пробирки, темнеет. Осадок имеет признаки сульфида меди. Сульфид меди обычно черного цвета, но в очень разбавленном растворе образовавшийся сульфид меди остается в коллоидном растворе. В присутствии электролитов он осаждается, образуя осадок бурого цвета, похожий на осадок медного касса. Еще более наглядно это видно при добавлении небольшого количества H2S в белое вино, содержащее медь и лишенное растворенного кислорода. При этом появляются муть и осадок сернистой меди красно-бурого цвета, растворимый в присутствии воздуха, как и осадок медного касса.
Анализы показали, что медь и сера находятся в некоторых осадках в таких же соотношениях, как и сернистая медь (CuS), но содержание серы иногда бывает меньше. Кроме того, осадок содержит небольшие количества неорганических веществ, фиксируемых адсорбцией (железо, кальций, фосфорная кислота), и особенно органических веществ, составляющих половину или больше общей массы осадка.
Муть и осадок медного касса представляют собой коллоидный сульфид меди, или коллоидную медь, или, что более вероятно, смесь обоих веществ. По одной гипотезе исчезновение мути при доступе воздуха объясняется окислением нерастворимого сульфида в растворимый сульфат меди. По второй гипотезе коллоидная сера, также очень окисляемая, заново образует ион двухвалентной меди Cu++. По той и по другой гипотезе механизм образования касса должен начинаться с восстановления солей двухвалентной меди, точнее с иона двухвалентной меди, и завершаться флокуляцией коллоида.
Если осаждается коллоидная металлическая медь, то осадок образуется из ионов двухвалентной меди Cu++ путем восстановления. Если же осаждается серная медь, серный ион получается от восстановления сернистокислого иона и такое восстановление происходит только в присутствии меди, предварительно восстановленной в ион одновалентной меди Cu+. В противном случае во всех сульфитированных винах, выдерживаемых без доступа воздуха, образуется сероводород и, следовательно, происходит осаждение коллоидной серы, как это показывает добавление сероводорода в вина, не содержащие меди. С другой стороны, при внесении в сульфитированные белые вина, содержащие медь, небольшого количества гуммиарабика, или же при подогревании их можно получить химический механизм медного касса без появления мути. В этом случае достаточно внести в вино немного желатины или рыбьего клея, чтобы реализовать флокуляцию коллоида двухвалентной меди, которая окрашивает в бурый цвет осадок белков.
Итак, механизм медного касса в общем виде можно схематически записать по первой гипотезе в виде следующих реакций:
1) Cu++ + RH ->- Cu+ + R + Н+— восстановление ионов двухвалентной меди;
2) 6Cu+ + 6Н+ + SO2 -> 6Cu++ + H2S+2H2O — восстановление сернистого ангидрида;
3) Cu++ + H2S ->- CuS + 2Н+ — образование серной меди;
4) флокуляция CuS под действием электролитов и белков с образованием мути и осадка.
По второй гипотезе восстановление Cu++ идет до стадии Cu, при этом восстанавливается SO2 в H2S. График на рис. 12.3 дает основание предполагать, что теоретически возможны оба механизма: восстановление иона Cu++ в ион Cu+ или в металлическую медь, причем более вероятен первый, когда pH вина высокий, и наоборот. Значения потенциала показаны лишь приближенно. Фактически потенциал системы Cu++/Cu+ равен 0,18 В (примерно величины предельного потенциала вин, изолированных от доступа воздуха в течение достаточно длительного времени). Этот предельный потенциал намного ниже нормального потенциала железа, что достаточно объясняет тот факт, что восстановление меди в вине намного труднее, чем восстановление железа, и в нормальных условиях и железо, и медь находятся в двухвалентных состояниях Cu II и Fe II, являющихся стабильными формами.
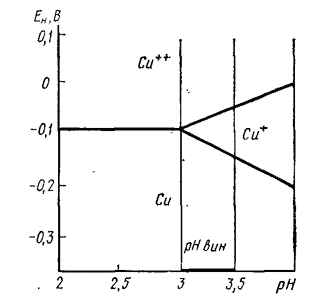
Рис. 12.3. Зависимость приближенных величин нормальных потенциалов окислительно-восстановительных систем меди от pH (по Шарло, 1957).
Внесение гуммиарабика, нагревание вина и обработка бентонитом противодействуют медному кассу или прекращают его полностью. Эти приемы представляют также и большой теоретический интерес, показывают роль защитных коллоидов, препятствующих флокуляции коллоида, содержащего двухвалентную медь, и роль белков вина, способствующих этой флокуляции. Гуммиарабик действует как защитный коллоид, бентонит удаляет флокулирующие белки, нагревание выполняет обе эти функции одновременно.
Работы, которые провели Кин и Марш, подчеркнули роль белков. В осадках, выделенных из коммерческих вин с медным кассом, было обнаружено высокое содержание азота и относительно мало сульфидных компонентов. Это наводит на мысль, что мутный осадок представляет собой медно-белковый комплекс, на котором адсорбированы другие компоненты. Медь необходима для образования обратимой мутности в синтетической среде. Сернистая кислота не является необходимой для образования реверсивной мутности, но она катализирует образование мутности при солнечном освещении всякий раз, когда в вине присутствуют медь и белки. Авторы приходят к заключению что мутность, которую обычно принимают за медный касс, в действительности представляет собой комплекс нескольких веществ: белок — танин, медь — белок и сульфид меди.
Обзор работ в этой области выполнил Марека Кортес (1963). В последнее время медный касс исследовал Вюрдиг (1969). Исследования механизма медного касса можно в основном подразделить на три части: а) Связь мутности с окислительно-восстановительным потенциалом; б) факторы и условия медного касса, состав мутного осадка и теория его образования; в) источники и состояние серы в осадках.
Американские авторы констатируют присутствие серы, меди и белков во всех осадках медного касса. Медь находится в состоянии сульфида, что предполагает восстановление иона двухвалентной меди в ион одновалентной меди и восстановление сернистой кислоты в сероводород h2s. Прямое восстановление представляется термодинамически возможным. Источником сернистого иона может быть сернистый ангидрид или белок. В первом случае американские авторы повторяют механизм, описанный в данной книге. Но сернистая кислота может также выполнять функцию агента, денатурирующего белок. В присутствии иона двухвалентной меди сернистая кислота восстанавливает связь дитиолцистина, чтобы образовать свободную сульфгидрильную группу цистеина. Ниже приводится реакция между сернистой кислотой и белками, дающая сульфат и белок с группами SH, способными присоединять медь:
H2SO3 + R — SS — R + H2O -> SO4 + 2R — SH + 3Н+.
При добавлении в белое вино с высоким содержанием меди (12,7 мг/л) бисульфита натрия, в который был введен радиоактивный изотоп S35, эти же авторы пытались определить в осадке медного касса долю серы, образующуюся из сернистой кислоты, и долю серы, происходящую из тиоловых групп белка. При солнечном свете специфическая радиоактивность серы, находящейся в осадке, такая же, как и у используемого бисульфита. Следовательно, в данном случае сернистая кислота восстанавливается в сульфид по приведенной выше схеме.
Белок не участвует в механизме восстановления, он оказывает действие только на флокуляцию. Напротив, когда касс образуется в темноте, часть серы осадка образуется из белка в результате его денатурации. Оба механизма возможны и нередко перекрывают друг друга.

