ОБЗОР ОБЩИХ СВЕДЕНИЙ О КОЛЛОИДАХ
Классификация дисперсных систем
Дисперсными системами, или дисперсиями, называют системы, составленные из какого-либо вещества, рассеянного в другом, в частности в жидкости, в состоянии тончайших частиц. Коллоидные дисперсии представляют собой системы, в которых вещество рассеяно в жидкости в состоянии крупных агрегатов маленьких молекул (или мицелл) или в состоянии больших молекул (или макромолекул), другими словами, в состоянии частиц определенных размеров — от обычных молекул до взвешенных частиц. Но классификация дисперсных систем по размерам частиц подходит только для частиц хотя бы приблизительно сферической формы и не годится для частиц удлиненной формы, как это часто бывает в органических коллоидах.
Таблица 11.1
Классификация дисперсных систем
Дисперсные системы | Размеры частиц, им | Число атомов в одной частице | Признаки частиц |
Молекулярные дисперсии (или ординарные растворы) | Приблизительно менее 2 | Менее 1000 | Проходят через бумажные и ультрафильтры; не видимы в. микрсскоп и в ультрамикроскоп; диффундируют и диализуются, не осаждаются |
Коллоидные дисперсии (или растворы). Частицы могут быть микрокристаллами, макромолекулами | Приблизительно от 2 до 100 | Между 1000 и 1 000 000 000 | Проходят через самый плотный, бумажный фильтр, но не проходят через ультрафильтры; не видимы в микроскоп, но в ультрамикроскопе видны, не диффундируют и не диализуются, осаждаются очень медленно |
Грубые дисперсии (или суспензии) | Приблизительно более 100 | Свыше | Не проходят через бумажный, фильтр, видны в микроскоп, не диффундируют и не диализуются; оседают очень быстро |
Указанные в табл. 11.1 пределы таких систем имеют производственный характер и не определяют ни конца одного вида частиц, ни начала другого. Между этими видами нет точных, определенных разграничительных линий: виден непрерывный переход между истинными растворами, коллоидными и суспензиями. Признаки, указанные в последней графе табл. 11.1, зависят одновременно от рассматриваемых веществ и технических условий, таких, как природа диализующей мембраны, размеры пор фильтров и разрешающие способности микроскопа. Известна целая гамма дисперсных систем, или гетерогенных растворов, и в этой шкале дисперсии, или коллоидные растворы, перемежаются с молекулярными растворами и суспензиями. Коллоидные свойства достаточно охарактеризованы только в центральной зоне коллоидных дисперсий с пределами, которые могут изменяться в зависимости от природы частиц.
Согласно Крюйти и Овербику (1961), коллоидные системы имеют частицы, размеры которых находятся в пределах от 1 до 1000 нм.
К группе коллоидов, способных образовывать коллоидные дисперсии, относят очень различные вещества, не имеющие никакой связи между собой по происхождению или составу (простые или очень сложные органические вещества), но которые имеют некоторые общие свойства. В этом отношении также нет четко обозначенной границы между коллоидами и неколлоидами (или «кристаллоидами», как говорили раньше). Некоторые вещества имеют в зависимости от условий те или иные свойства. Например, хлористый натрий и многие другие соли дают с водой истинные, или молекулярные растворы. Но при более или менее значительном добавлении спирта они дают коллоидные растворы со всеми степенями дисперсий, промежуточных между молекулярным раствором и осадком. Точно так же и фенольные соединения могут быть в истинном растворе или в коллоидном.
В качестве примера можно, сказать, что глины, такие, как каолин и бентонит (которые используются для обработки вина), образуют в воде мутные суспензии, размеры частиц которых значительно больше, чем у коллоидных гранул, вплоть до 2 мкм. Но в действительности эти гранулы образуются из частиц кремния и алюминия, наложенных одна на другую на расстоянии (примерно 1 нм), соответствующем точно величине коллоидных частиц. Жидкость проникает в промежуток между частицами и обменивается с ними некоторыми из своих компонентов. Эти обмены происходят намного легче у монморилонита, чем у каолинита, частицы которого намного больше сближены и связаны между собой. Можно сказать, что коллоидные свойства выражены в большей степени у монморилонита, который поглощает много воды, сильно набухает и фиксирует много ионов из раствора. По своим свойствам он ближе к гидрофильным коллоидам, тогда как каолинит ближе к гидрофобным коллоидам.
Основные понятия
Терминология науки о коллоидах и коллоидных явлениях все еще неточна, и значения отдельных терминов изменяются в зависимости от автора. Ниже будут упоминаться такие термины и выражения, которые, по мнению авторов настоящей книги, лучше всего подходят для описания и объяснения коллоидных явлений, встречающихся в энологии.
Как правило, коллоиды могут находиться в состоянии коллоидных растворов (называемых также золями, или псевдорастворами) или в состоянии гелей. Золь обладает текучестью, небольшой вязкостью, не затвердевает; частицы не связаны одна с другой и находятся в спонтанном, беспорядочном движении, называемом броуновским, которое вызывается столкновением соседних молекул. Гель, наоборот, характеризуется тем, что в этом состоянии частицы неподвижны одна относительно другой, группируются в более или менее крупные скопления. Такие связи препятствуют броуновскому движению. Гель обладает жесткостью и гибкостью и ведет себя, как настоящее твердое тело. Он состоит из ткани, которую можно сравнить с сеткой взаимно переплетающихся фибровых нитей и ячеек, наполненных жидкостью. Желе (или гелем, студнем) называют аморфные вещества, (желатина, крахмал, агар, каучук и др.), которые набухают при погружении в соответствующую жидкость.
Под пептизацией понимают переход коллоида из состояния геля в состояние золя. Этот процесс можно сравнить с растворением геля. Флокуляция означает переход из состояния золя в состояние геля. Ее можно сравнить с осаждением соли; частицы, первоначально свободные, слипаются и стремятся выйти из жидкости, образуя хлопья, являющиеся кусками геля. Термин «осаждение» означает всякое отделение растворенного вещества от растворителя в любой форме; тонкий осадок, кристаллизованный или нет, большего или меньшего объема, делающий жидкость мутной, или оседающей, видимый на глаз. В случае коллоидов этот термин часто используют в том же смысле, что и термин «флокуляция». Под термином «коагуляция» понимают переход из состояния золя в состояние геля; частицы агломерируются внутри жидкости, но не в отдельные хлопья, как при флокуляции, а в одну сплошную массу; происходит охватывание коллоида без разделения на две фазы, как при флокуляции. Термин «синерезис» означает переход из состояния желе в состояние геля. Масса коллоида претерпевает сжатие, сокращается в размерах с выталкиванием большей части инертного вещества, который находился в желе, следовательно, желе дает две фазы.
Схема, изображенная на рис. 11.1, дает представление об изложенных: выше определениях.
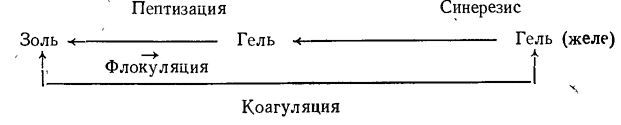
Рис. 11.1. Схема коллоидных превращений.
Флокуляция есть не что иное, как сумма коагуляции и синерезиса: сначала происходит застудневание, затем ослабление этого желе в результате разрыва и контрактации его сетки. Хлопья геля всего лишь обломки, куски этой разрушенной массы, которая выталкивает растворитель с одновременным сокращением своего объема. Многие гели в действительности представляют собой желе, набухшее до крайних размеров; они как бы разламываются от чрезмерного разбухания, поскольку внутренние связи оказываются недостаточно прочными. Фактически при оклейке вин коагуляция и синерезис могут в некоторых условиях протекать совершенно раздельно: сначала затвердевание (схватывание), затем разрыв массы путем перемешивания.
Другие авторы применяют названия гель и желе, флокуляция и коагуляция в более или менее различном смысле. Некоторые применяют только термины «гель» и «осаждение»; при этом гель означает все состояния, в которых коллоид находится в более или менее твердом, эластичном, жестком состоянии, а осаждение означает все разделения коллоида и жидкости. В исследовании по оклейке вин удобно использовать термин «флокуляция» для обозначения осаждения в форме видимых на глаз хлопьев, которое обычно» сопровождается осаждением хлопьев и осветлением жидкости. К тому же флокуляцией в просторечии называют «осаждение некоторых коллоидных растворов в виде хлопьев». Такая неопределенность терминов ведет к неправильным представлениям о сложной структуре гелей и желе.

