Сернистый ангидрид обладает некоторыми очень важными свойствами, благодаря которым он является исключительно ценным консервирующим средством. С одной стороны, сернистый ангидрид эффективно противодействует развитию всех микроорганизмов в вине: дрожжей, молочнокислых и уксуснокислых бактерий и, таким образом, предотвращает образование дрожжевой мути, вторичное брожение сладких вин, развитие Micoderma vini и образование цвели, сбраживание бактериями сахаров, органических кислот, глицерина, уксуснокислое брожение. С другой стороны, сернистый ангидрид легко окисляется или, что то же самое, будучи сильным восстановителем, предохраняет вина от слишком интенсивного окисления некоторых полифенолов, участвующих в образовании аромата, предотвращает мадеризацию; способствует установлению низкого уровня окисления-восстановления, благоприятствующего развитию вкусовых качеств вина; связываясь с ацетальдегидом, сернистый ангидрид не допускает потери букета вином в результате избыточной аэрации. Наконец, хорошо известны его антиоксидазные свойства; он ингибирует и разрушает тирозиназу и лакказу, не допускает развития оксидазного касса (серьезного дефекта белых и красных вин), препятствует появлению даже слабых проявлений оксидазного помутнения. В конечном счете, сернистый ангидрид представляет собой хороший антисептик, ценное антиокислительное средство и эффективный фактор улучшения вина.
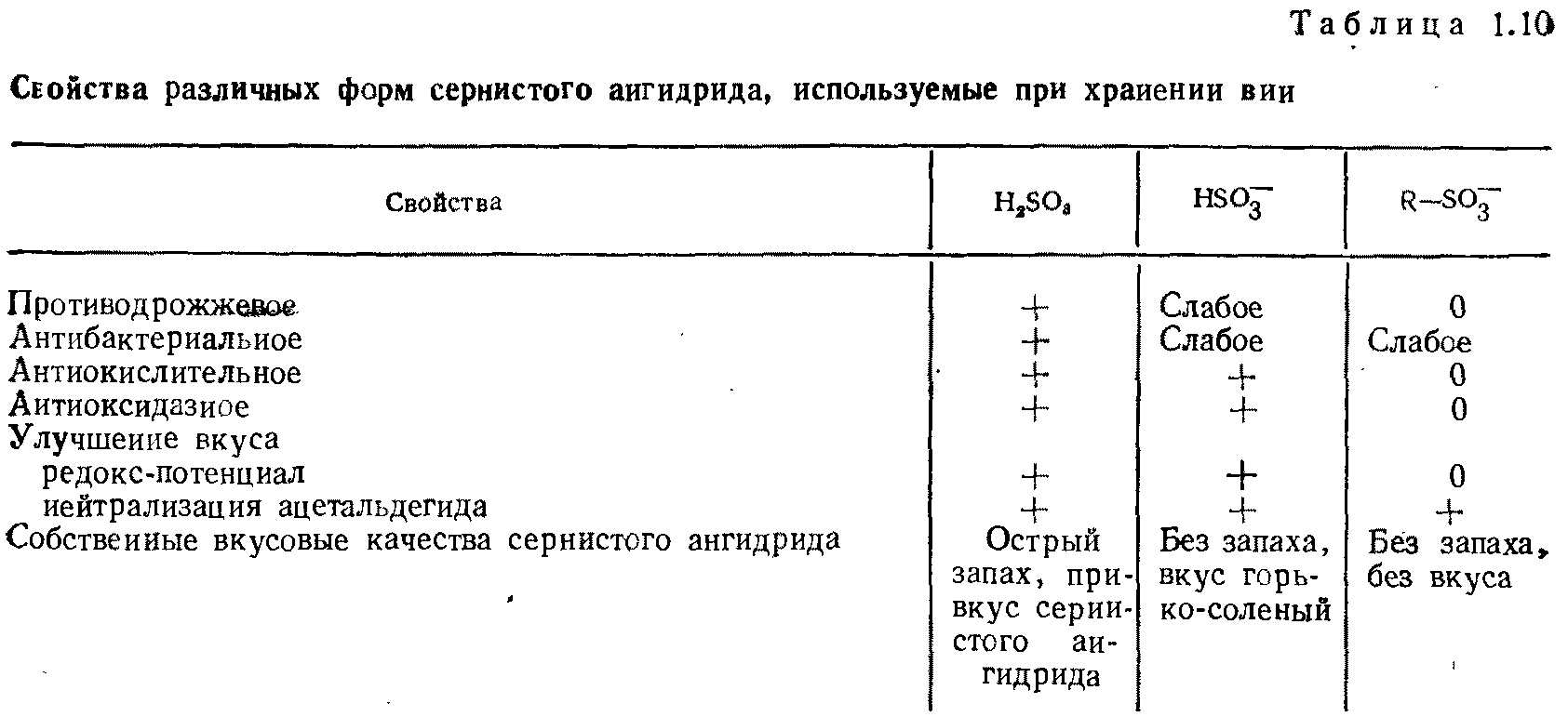
Следует иметь в виду, что все эти свойства не относятся к разнообразным формам, в которых сернистый ангидрид находится в винах. В табл. 1.10 приведены различия в активности SO2, которые не всегда учитывали.
Противодрожжевая активность
Эта активность обеспечивается почти полностью недиссоциированной молекулой H2SO3. По наблюдениям, которые сделали Реэм и Виттмани (1962, 1963), H2SO3 в 100—500 раз более активна на Sacch. cerevisiae, чем HSO3. Однако не следует смешивать активность фунгицидную с фунгистатической.
В табл. 1.11 приведены результаты опыта, который хорошо показывает влияние pH на антисептическую активность сернистого ангидрида. Суспензия дрожжей или бактерий, помещенная в фосфатные буферные растворы при pH 3,0 и 3,8, получает возрастающие количества SO2. Полученную смесь оставляют в покое в течение 6 ч без доступа воздуха, затем наносят на чашку Петри с разбавлением, необходимым для подсчета оставшихся живых клеток.
Установлено, что влияние pH на активность сернистого ангидрида сильнее проявляется в отношении бактерий, чем дрожжей. Раствор при pH 3,0 содержит в 5,9 раза больше H2SO3, чем такой же раствор при pH 3,8. Если по этим данным трудно вычислить антисептический эффект H2SO3 и НSO3, то, очевидно, H2SO3 менее бактерицидна, тогда как она представляется здесь довольно фунгицидной.
Таблица 1.11
Антисептическое действие сернистого ангидрида на Sacch. ellipsoideus и на Leuconostoc gracile в зависимости от pH
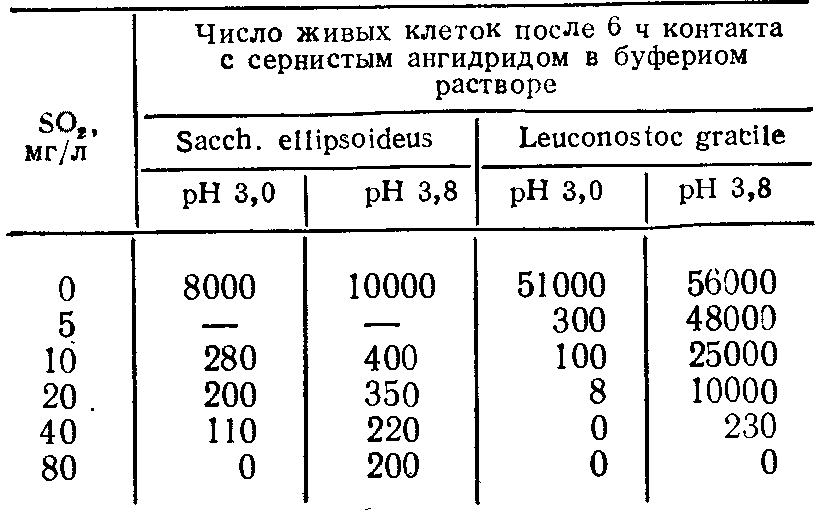
Таблица 1.12
Содержание свободного сернистого ангидрида (в мг/л), которое необходимо для поддержания в винах антисептической активности, равной активности 2 мг SO2 (в виде H2SO3)

Различные расы дрожжей и молочнокислых бактерий вина обладают неодинаковой восприимчивостью к различным формам сернистого ангидрида, поэтому при определении активных доз его для использования в зависимости от pH таблицы эквивалентности составляют весьма приближенно (табл. 1.12). Вычислены величины содержания свободного SO2 (титруемые непосредственно йодом), к которым следует приводить вина в зависимости от их pH, чтобы обеспечить антисептическую активность, равную активности 2 мг/л сернистого газа (SO2 или H2SO3). Известны различные гипотезы, согласно которым бисульфитная форма HSO3 обладает в большей или меньшей степени антисептической активностью. Если исходить из того, что HSO3 не имеет активности или же она в 100, 20 или 10 раз меньше, чем у формы H2SO3, величины содержания свободного SO2, которые следует поддерживать в вине, будут соответственно в 9,5, 2,3 и 1,8 раза больше при pH 3,8, чем при pH 2,8. Данные опыта, проведенного при хранении вин, в частности вин, содержащих восстанавливающие сахара, по-видимому, согласуются со значениями в том случае, когда НSO3в 20 раз менее активен, чем H2SO3. Но для разработки этой проблемы, видимо, потребуются дальнейшие систематические исследования. Нужно дифференцировать фунгицидную активность, которая завершается разрушением клетки, и активность фунгистатическую, которая является обратимой. Сернистый ангидрид фунгистатичен при высоком pH и в малых дозах и фунгициден при низком pH и в больших дозах. Форма HSO3 определенно является фунгистатической ; она не имеет фунгицидных свойств.
С другой стороны, SO2 в связанной форме не обладает никакой противодрожжевой активностью (Реэм и сотрудники, 1965). Стало привычным считать, что дрожжи инактивируют SO2, высвобождая ацетальдегид, который быстро переходит в состояние неактивной альдегидосернистой кислоты.
Действие SO2 на дрожжи во время сульфитации происходит не мгновенно, а с постепенным нарастанием. Это доказано на следующем опыте. Бродящее виноградное сусло сульфитируют все возрастающими дозами SO2 (от 100 до 350 мг/л). Подсчитывают живые клетки и общее количество дрожжей через различные промежутки времени. После внесения 100 мг/л создается впечатление, что брожение внезапно останавливается. Во всяком случае, концентрация сахара остается постоянной, хотя точные манометрические измерения выявляют в течение еще 1 ч выделение углекислого газа.
Через 1 ч после сульфитации активность дрожжей еще не прекращается, поскольку они в целом еще продолжают размножаться, какими бы ни были применяемые дозы. Через 5 ч популяция обычно уже сильно подавлена. Из 58 000 клеток на 1 мм3 после добавления 100 мг/л SO2 остается живых 8000, после добавления от 150 до 250 мг — 3000 и при внесении 300 мг/л — всего 1080. Через 24 ч после сульфитации действие SO2 на дрожжи еще более усиливается. Лишь 30 клеток на 1 мм 3 способны образовывать колонии в присутствии 100 мг/л SO2. При более высоких дозах SO2 практически все клетки теряли способность к самовоспроизводству. В действительности всегда остается несколько живых клеток, даже если кажется, что они потеряли на короткое время способность образовывать колонии. Чтобы убедиться в этом, достаточно засеять небольшой объем стерильного виноградного сусла каплей среды (сульфитированной 350 мг/л SO2), в которой все дрожжевые клетки казались лишенными жизни. Через два дня это сусло обнаруживает признаки активного брожения.
Следовательно, сульфитация не вызывает немедленного разрушения всех дрожжевых клеток. Действие ее происходит не внезапно. Лишь постепенно, как наркотик, она достигает всех клеток. Вначале она блокирует ферменты, останавливая, таким образом, химические процессы брожения. Все происходит так, как если бы SO2 фиксировался на дрожжевых клетках. Для некоторого определенного количества дрожжей ингибирование бывает полным, и клетки отмирают. В этом случае SO2 производит фунгицидное действие, у другой, меньшей части, клетки остаются живыми, но временно лишенными своих функций брожения и воспроизводства. Здесь SO2 является только фунгистатическим. При этом ингибирование имеет обратимый характер: если содержание свободного SO2 падает ниже некоторого уровня, дрожжи возобновляют свою активность. Биологическая стабильность зависит от некоторого равновесия между содержанием активного SO2 и числом клеток среды. Если первое снижается при окислении, а второе возрастает при засеве, брожение возбуждается без какой-либо задержки.
Бактерицидное действие
Антибактериальная активность свободного SO2 хорошо известна, и еще недавно считали, что это его единственная активная форма. Выше было отмечено, что связанный SO2 также обладает своим собственным ингибирующим действием.
Сначала Форнашон (1963) отметил, что в присутствии альдегидосернистой кислоты некоторые гетероферментативные бактерии потребляли альдегидную часть соединения, высвобождая, таким образом, достаточные количества SO2, чтобы прекратить дальнейший рост бактерий.
С. Лафон-Лафуркад и Пейно (1974) установили, что фактически SO2 далеко не инертный биологически, когда связан с ацетальдегидом или с пировиноградной кислотой, сам по себе обладает антибактериальной активностью, которой нельзя пренебрегать. Бактерицидное действие особенно заметно, когда SO2 в связанной форме находится в контакте с популяциями бактерий и когда не происходит высвобождения его. Кроме того, связанный SO2 задерживает рост бактерий и тормозит яблочно-молочное брожение (рис. 1.13). SO2 оказывает даже прямое влияние на ферментативные процессы последнего.
Из этих наблюдений можно заключить, что бактерицидные свойства SO2 имеют большое технологическое значение для проведения яблочно-молочного брожения и хранения вин.
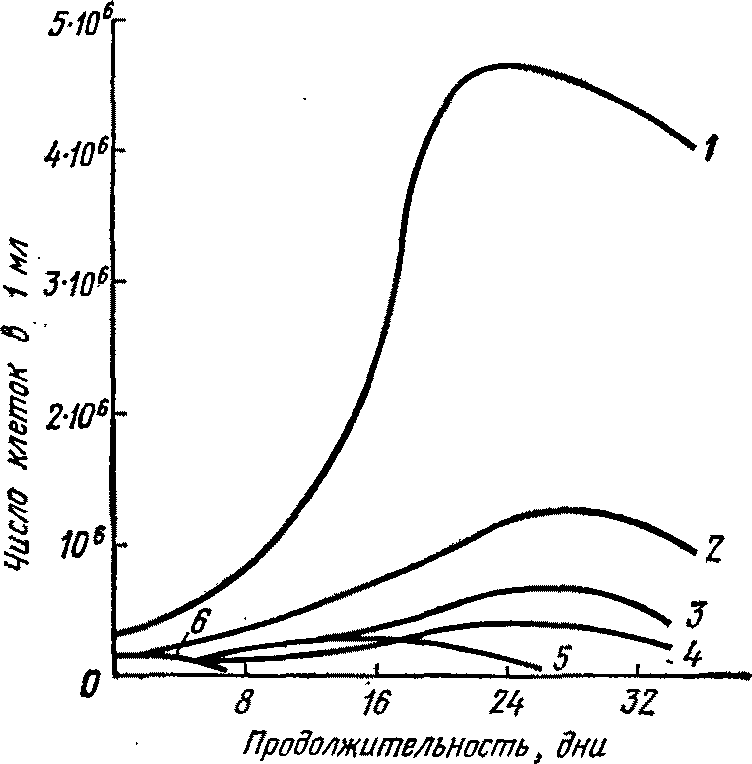
Рис. 1.13. Действие свободного сернистого ангидрида, а также связанного с ацетальдегидом и пировиноградной кислотой на рост Leuconostoc gracile в вине:
1 — контроль; 2 — +10 мг/л сернистого ангидрида, связанного с ацетальдегидом; 3 — +10 мг/л сернистого ангидрида, связанного с пировиноградной кислотой; 4 — +10 мг/л сернистого ангидрида в свободном состоянии; 5 — +30 мг/л сернистого ангидрида, связанного с ацетальдегидом; 6 — +30 мг/л сернистого ангидрида, связанного с пировиноградной кислотой.
Сульфитирование мезги действует на бактерии не только в течение короткого периода до начала брожения. В действительности действие сульфитации проявляется прежде всего в том, что в вине остается некоторое количество SO2 в связанной форме, который осуществляет эффективную защиту вина в течение всего времени хранения.

